Gomisin N inhibuje melanogenézu prostredníctvom regulácie signálnych dráh PI3K/Akt a MAPK/ERK v melanocytoch
Mar 17, 2022
Kontakt:joanna.jia@wecistanche.com/ WhatsApp: 008618081934791
Abstrakt: Gomisin NV rôznych štúdiách sa preukázalo, že jedna z lignanových zlúčenín nachádzajúcich sa v Schisandra Chinensis má antioxidačné, protinádorové a protizápalové účinky. Po prvýkrát tu uvádzame antimelanogénnu účinnosť Gomisinu N u cicavcov. ako aj v embryách zebričiek. Gomisin N významne znížil obsah melanínu bez bunkovej toxicity. Hoci nebol schopný modulovať katalytickú aktivitu húbtyrozinázain vitro,Gomisin Ndownreguloval hladiny expresie kľúčových proteínov, ktoré fungujú vmelanogenéza. Gomisin N downreguloval receptor melanokortínu 1 (MC1R), adenylylcyklázu 2, transkripčný faktor spojený s mikroftalmiou (MITF), tyrozinázu,tyrozinázapríbuzný proteín-1(TRP-1) a proteín súvisiaci s tyrozinázou-2 (TRP-2). Okrem toho bunky Melan-A ošetrené Gomisinom N vykazovali zvýšené hladiny p-Akt a p-ERK, čo znamená, že aktivácia dráh PI3K/Akt a MAPK/ERK môže fungovať tak, že inhibujemelanogenéza. Tiež sme potvrdili, že Gomisin neznížil produkciu melanínu potlačením expresie MITF,tyrozináza, TRP-1 a TRP-2v myších a ľudských bunkách, ako aj vo vyvíjajúcich sa embryách zebričiek. Spoločne sme dospeli k záveru, žeGomisin Ninhibuje syntézu melanínu potlačením expresie MITF a melanogénnych enzýmov, pravdepodobne prostredníctvom modulácie dráh PI3K/Akt a MAPK/ERK.
Kľúčové slová:Schisandra Chinensis;Gomisin N; lignan;melanogenéza; bielenie kože

cistanche majú funkciu bielenia pokožky
1. Úvod
Melanín je pigment nachádzajúci sa vo väčšine zvieracích orgánov vrátane kože, vlasov, očí, vnútorného ucha, kostí, srdca a mozgu [1,2].Melanogenézaje komplexný proces, v ktorom sú zapojené viaceré signálne dráhy. Receptor melanokortínu 1 (MC1R) je kľúčovým regulátorom vmelanogenézasignalizáciu prostredníctvom svojich ligandov, ako je hormón stimulujúci melanocyty (MSH) a adrenokortikotropný hormón (ACTH) [3]. Kožný melanín je biosyntetizovaný melanocytmi v epiderme a potom prenesený do keratinocytov, kde zohráva dôležitú úlohu pri ochrane kože tým, že absorbuje UV žiarenie zo slnečného žiarenia a zachytáva reaktívne voľné radikály [4,5]. Syntéza a prenos melanínu v koži a vlasových folikuloch je regulovaná dostupnosťou jeho prekurzorov [6]. L-tyrozín a L-dihydroxyfenylalanín (L-DOPA), hlavné substráty melanogénnych enzýmov, tiež fungujú ako regulátory podobné hormónom v melanogenéze [7]. Na druhej strane nadprodukcia melanínu vedie k nežiaducim kožným problémom, ako sú pehy a melazma [8,9]. Melanogenéza môže ovplyvniť správanie normálnych a malígnych melanocytov moduláciou elastických vlastností buniek [10]. Hoci receptory serotonínu a melatonínu exprimované v kožných bunkách hrajú kľúčovú úlohu pri udržiavaní bunkovej homeostázy, nadmerná produkcia melanínu prostredníctvom nekontrolovaných hormonálnych zmien môže spôsobiť patologické stavy v koži [11].
Existovalo teda rozsiahle úsilie na objasnenie molekulárnych mechanizmov, ktoré kontrolujú melanogenézu ako primárny krok pri liečbe hyperpigmentárnych kožných porúch. Okrem toho rôzne druhybielenie kožečinidlá, ktoré inhibujú syntézu melanínu, boli identifikované z rastlinných a nerastlinných extraktov a komerčne používané v kozmeceutikách [12,13]. Medzi najpoužívanejšie bieliace činidlá patria hydrochinón, mechinol, arbutín, kyselina kojová, kyselina askorbová a kyselina retinová [12,14]. Avšak existujú rôzne obmedzenia ich použitia pri liečbe akútnych alebo chronických symptómov hyperpigmentácie u ľudí. Napríklad hydrochinón, hoci sa na depigmentáciu používa už od 60. rokov 20. storočia, môže spôsobiť podráždenie kože a kontaktnú dermatitídu [15,16]. Vedie tiež k poškodeniu DNA zvýšením produkcie reaktívnych foriem kyslíka a rozvojom exogénnej ochronózy v bunkách cicavcov [17,18]. Iné známetyrozinázaInhibítory ako kyselina kojová a kyselina askorbová majú nielen slabú penetráciu kožou, stabilitu a bieliacu účinnosť, ale pri dlhodobom používaní môžu spôsobiť aj cytotoxicitu, dermatitídu a erytém [19,20]. V tomto ohľade narastá potreba vyvinúť bezpečnejšie a účinnejšie bieliace činidlá na liečbu hyperpigmentácie ľudskej pokožky. Prírodné byliny používané v tradičnej medicíne môžu poskytnúť alternatívne zdroje na identifikáciu nových bieliacich činidiel, ktoré riadia kľúčové krokymelanogenézas menšími alebo žiadnymi vedľajšími účinkami [21].
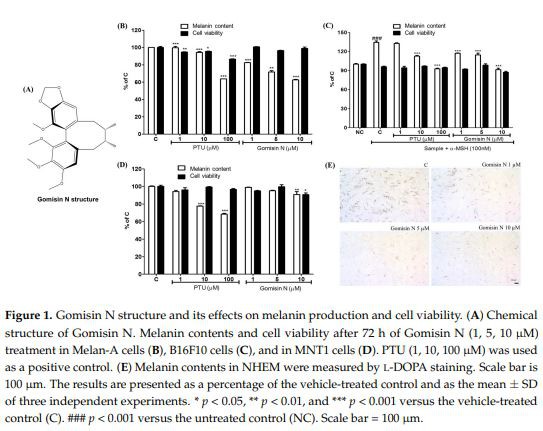
Schisandra chinensis, tiež známa ako severské bobule jemnej chuti, sa prirodzene vyskytuje v severovýchodnej Číne, na ďalekom východe Ruska, Japonsku a Kórei [22]. Táto rastlina sa v tradičnej orientálnej medicíne už dlho používa na liečbu šeroslepoty, popálenín kože, aseptických zápalov a ochorení pečene [23,24]. Ukázalo sa, že extrakt z ovocia S. chinensis a jeho lignanové zlúčeniny majú rôzne farmakologické účinky na myšacie bunkové línie. Napríklad Schisandra A a C má antioxidačné účinky, zatiaľ čo Schisandra B má antifibrotické, protizápalové, antioxidačné a antiapoptotické účinky [25]. Ďalšia lignanová zlúčeninaGomisin N(Obrázok 1A) sa uvádza, že potláča apoptózu indukovanú oxidačným stresom inhibíciou uvoľňovania cytochrómu C z mitochondrií do cytoplazmy, štiepenia kaspázy 3 a PARP a prechodu mitochondriálnej permeability indukovaného Ca2 plus v kardiomyocytoch potkanov H9c2 [7,8]. Je zaujímavé, že niekoľko štúdií s použitím myších modelov a ľudských kožných bunkových línií odhalilo terapeutický potenciál S. chinensis pri liečbe kožných porúch. Lee a kol. uviedli, že metanolový extrakt z plodov S. chinensis zmierňuje symptómy kontaktnej dermatitídy znížením produkcie prozápalových cytokínov, ako sú TNF- a IFN- pri lokálnej aplikácii [8,24]. Kang a kol. ukázali, že vodný extrakt Schisandra Fructus inhiboval aktiváciu IκB, čím potláčal produkciu TNF-, IL-6 a GM-CSF v línii ľudských žírnych buniek HMC-1 [26]. Tieto zistenia nás viedli k predpokladu že lignany S. chinensis by mohli ovplyvňovať funkcie kožných buniek širšie. V tejto štúdii sme sa snažili preskúmať domnelé úlohyGomisin N, jedna z hlavných lignanových zlúčenín v S. Chinensis, pri reguláciimelanogenéza, čím sa vyhodnotí jeho potenciálne použitie ako kozmeceutického činidla. Tu to hlásimeGomisin Ninhibuje biosyntézu melanínu bez bunkovej toxicity v ľudských a myších bunkách, ako aj v embryách zebričiek.
2. Výsledky
2.1. Účinky Gomisinu N na tvorbu melanínu a životaschopnosť buniek
Na overenie účinkov Gomisinu N namelanogenéza, ošetrili sme myšacie melanocyty s rôznymi koncentráciamiGomisin N72 hodín a potom sa vyhodnotili zmeny v obsahu melanínu. Liečba gomisínom znížila obsah melanínu v normálnej bunkovej línii melanocytov Melan-A aj v bunkách melanómu B16F10 spôsobom závislým od dávky bez bunkovej toxicity (obrázok 1B, C). Pozorovali sme, že Gomisín N inhiboval -MSH-indukovanú produkciu melanínu v B16F10 bunkách, čo bolo porovnateľné s výsledkami získanými ošetrením PTU [27] (obrázok 1C). Vyhodnotiť, či došlo k zníženiu hladiny melanínuGomisin Nliečba je spôsobená zníženou aktivitou tyrozinázy, vykonali sme test farbenia L-DOPA v normálnych ľudských epidermálnych melanocytových (NHEM) bunkách. Ako je znázornené na obrázku 1E, bunky NHEM ošetrené Gomisínom N vykazovali znížené hladiny L-DOPA v porovnaní s neošetrenými bunkami. Inhibičný účinok Gomisínu N na produkciu melanínu však nebol významný v bunkách ľudského melanómu MNT-1 (obrázok 1D) .

2.2. Účinky Gomisinu N na aktivitu tyrozinázy
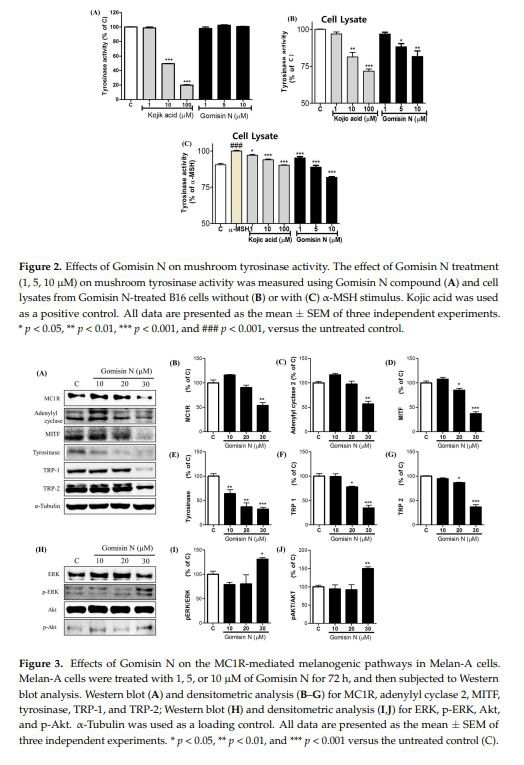
Skúmať, čiGomisin Nbrzdítyrozinázain vitro sme použili hubovú tyrozinázu a bunkové lyzáty melanómu B16. Kyselina kojová, dobre známy inhibítor tyrozinázy, sa použila ako pozitívna kontrola. Keď sa ošetril hubovou tyrozinázou, zatiaľ čo kyselina kojová významne znížila enzymatickú aktivitu, Gomisín N neindukoval žiadnu zmenu v premene L-DOPA na dopachróm (obrázok 2A). Avšak, keď bol ošetrený na bunky melanómu B16, Gomisín N viedol k zníženiu vtyrozinázaaktivita bunkového lyzátu spôsobom závislým od dávky (obrázok 2B). Navyše, keď sa súčasne ošetrili s bunkami -MSH inB16,Gomisin Nzvrátil zvýšenie tvorby dopacrómu stimulovaného -MSH (obrázok 3C). Predovšetkým sa zdá, že Gomisín N je účinnejší ako kyselina kojová pri inhibícii bunkovejaktivitu tyrozinázyB16 buniek po stimule -MSH. Tieto zistenia naznačujú, že inhibičný účinok GomisinN na produkciu melanínu pozorovaný v myších a ľudských bunkách (obrázok 1) nie je spôsobený jeho funkciou priamo inhibovať katalytickú aktivitu tyrozinázy. Stále je však možné, že Gomisín N reguluje expresiu tyrozinázy alebo iných proteínov, ktoré hrajú kľúčovú úlohu vmelanogenéza.
2.3. Účinky Gomisinu N na inaktiváciu signálnej dráhy MC1R
Snažili sme sa objasniť základný mechanizmus zodpovedný za inhibičný účinok GomisinN na produkciu melanínu. Zdôvodnili sme toGomisin Nmôže regulovať signálne proteíny, ktoré sú zahrnutémelanogenézaa tým inhibujú syntézu melanínu. Receptor melanokortínu 1 (MC1R) je receptor spojený s amelanocytárnym G proteínom, ktorý funguje ako kľúčový regulátor pri syntéze melanínu. Aktivácia MC1R jeho ligandom -MSH alebo adrenokortikotropným hormónom (ACTH) vedie k zvýšeniu adenylylcyklázy, ktorá následne zvyšuje intracelulárne hladiny cAMP [2,3]. V dôsledku toho sa transkripčná hladina MITF zvyšuje prostredníctvom dráhy proteínkináza-C (PKA)/responzívny prvok viažuci proteín (CREB) [2,28]. Aby sme vyhodnotili regulačný účinok Gomisinu N na signalizačnú dráhu MC1R, skontrolovali sme hladiny expresie MC1R a jeho downstream signálnych molekúl po ošetrení buniek Melan-A pomocou Gomisinu N. Zistili sme, že Gomisin N významne znížil hladiny proteínov MC1R aj adenylylcyklázy 2. spôsobom závislým od dávky (obrázok 3A–C). Ako sa očakávalo,Gomisin N-ošetrené bunky tiež vykazovali znížené hladiny proteínov MITF a jeho známych cieľov tyrozinázy, TRP-1 a TRP{2}} (obrázok 3A, D–G). Tieto zistenia naznačujú, že Gomisin N inhibuje enzýmy produkujúce melanín inaktiváciou MITF prostredníctvom signálnej dráhy MC1R.
2.4. Účinky Gomisinu N na fosforyláciu Akt a ERK1/2 v bunkách Melan-A
Je známe, že dráhy PI3K/Akt a MAPK/ERK sa podieľajú na melanogenéze prostredníctvom transkripčnej alebo post-transkripčnej regulácie MITF [29,30]. Aby sme vyhodnotili, či GomisinN ovplyvňuje tieto signálne dráhy, hodnotili sme stav fosforylácie Akt a ERK1/2 analýzou Western blot. Ako je znázornené na obrázku 3H-J, ošetrenie vysokou dávkou (30 uM)Gomisin Nvýznamne zosilnili fosforyláciu Akt aj ERK. Tieto údaje naznačujú, že inhibičný účinok Gomisinu N namelanogenézapravdepodobne súvisí s dráhami P13K/Akt a MAPK/ERK.
2.5. Gomisin N inhiboval melanogenézu v embryách zebričiek
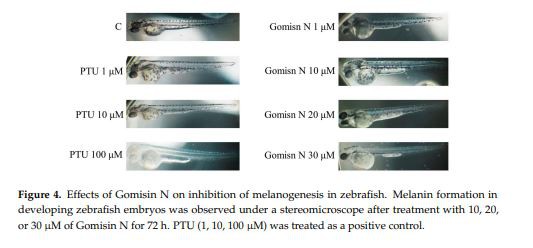
Ďalej sme sa zamerali na skúmanie, či je Gomisin N účinný pri inhibíciimelanogenézain vivo. Za týmto účelom sme embryá zebrafish ošetrili Gomisinom N počas 72 hodín v koncentráciách 1, 10, 20 a 30 uM a potom sme merali hladiny expresie melanogénnych proteínov. Pozorovali sme, že liečba Gomisinom N inhibovala tvorbu melanínu vo vývoji embryí zebričiek.Gomisin N-ošetrené embryá vykazovali zníženie obsahu melanínu spôsobom závislým od koncentrácie v porovnaní s neošetrenou kontrolou (obrázok 4). Zistili sme tiež, že hladiny bielkovíntyrozináza, MITF, TRP{0}} a TRP{1}} sa liečbou Gomisinom N znížili (obrázok 5). Tieto výsledky ukazujú, že Gomisin N inhibuje melanogenézu in vivo reguláciou transkripčného faktora MITF a jeho cieľovtyrozináza, TRP-1 a TRP-2.

2.6. Gomisín N zvrátil rapamycínom indukovanú melanogenézu v ľudskom MNT-1
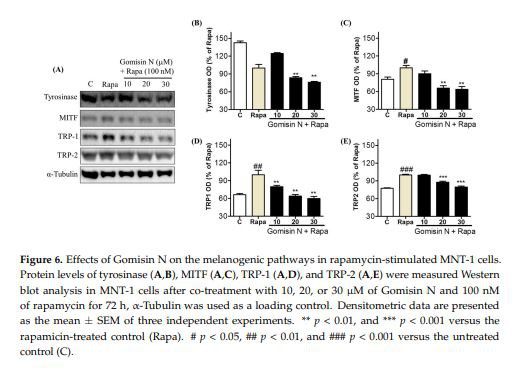
Hoci Gomisin N výrazne inhibovalmelanogenézav bunkách Melan-A a B16, ako aj embryách inzebrafish, sme nepozorovali jeho účinok na bunky ľudského MNT-1 melanómu. Očakávali sme, že účinok Gomisinu N môže byť detegovateľný v MNT-1 bunkách za podmienok, keď je melanogenéza regulovaná vhodným stimulom. Ukázalo sa, že rapamycín indukuje melanogenézu zvýšením aktivity tyrozinázy a hladín proteínov MITF, tyrozinázy, TRP-1 a TRP-2 [31], čiastočne prostredníctvom aktivácie autofágie [32]. Sledovali sme hladinytyrozináza, MITF, TRP-1 a TRP{1}} v bunkách MNT-1 pomocou analýzy Western blot, po spoločnej liečbe s Gomisinom N andrapamycínom. Liečba rapamycínom významne indukovala hladiny MITF, TRP-1 a TRP{5}}, ale nemala žiadny vplyv natyrozinázaúrovne (obrázok 6). Liečba Gomisinom N však významne zvrátila účinky rapamycínu na MITF, TRP-1 a TRP-2 spôsobom závislým od koncentrácie. Opačný účinokGomisin Nproti rapamycínu bol sľubnejší pri koncentrácii 20 a 30 uM ako 10 uM. Tieto výsledky naznačujú, že Gomisin N inhibujemelanogenézav ľudských MNT-1 melanómových bunkách reguláciou transkripčného faktora MITF a jeho cieľov TRP-1 a TRP-2.
3. Diskusia
Hlavnou funkciou melanínu je ochrana kožných buniek pred UV žiarením [33–35]. Hyperpigmentácia, dôsledok nadprodukcie melanínu v koži, spôsobuje nežiaduce kozmetické problémy a je spojená s dermatitídou a rakovinou kože. Naznačilo to niekoľko správmelanogenézaako dôležitý cieľ liečby metastatického melanómu [36,37]. Existuje teda rastúca potreba vyvinúť antimelanogénne činidlá, ktoré regulujú melanogenézu bez bunkovej toxicity [38]. Na melanogenéze kože sa podieľa niekoľko dráh [39,40]. Po väzbe ligandu MC1R zvyšuje aktivitu adenylylcyklázy, ktorá následne zvyšuje intracelulárne hladiny cAMP [41,42]. O cAMP-dependentnej aktivácii PKA/CREB dráhy sa často uvádza, že zvyšuje transkripčné hladiny MITF, čím zvyšuje syntézu melanínu [43]. MITF funguje ako hlavný regulátor troch hlavných melanogénnych enzýmov tyrozinázy, TRP-1 a TRP-2u stavovcov [3,21,44]. Tieto enzýmy sú transmembránové proteíny umiestnené v melanozomálnej membráne melanocytov. Tyrozináza reguluje krok obmedzujúci rýchlosťmelanogenézakonverziou L-tyrozinázy na L-DOPA [23]. TRP-1 a TRP{4}} tiež zohrávajú dôležitú úlohu pri syntéze melanínu, hoci ich funkcie nie sú úplne pochopené.
V tejto štúdii Gomisin N, lignanová zlúčenina S. chinensis, vykazoval depigmentačnú aktivitu bez bunkovej toxicity. Gomisin N inhiboval syntézu melanínu v kultivovaných cicavčích bunkových líniách, ako aj v embryách zebričiek. Gomisín N sa zdal byť účinnejší ako pozitívna kontrola PTU inhibujúca produkciu melanínu v bunkách Melan-A (obrázok 1B). Gomisin N znižoval obsah melanínu spôsobom závislým od koncentrácie. V porovnaní s neošetrenou kontrolnou skupinou, 10 uMGomisin Nznížil obsah melanínu asi o 40 percent, bez bunkovej toxicity. Antimelanogénna aktivita 10-uM Gomisinu N bola porovnateľná s aktivitou 100-uM PTU v bunkách Melan-A. Podobne sa Gomisin zdal byť účinnejší ako PTU v bunkách B16F10 aktivovaných -MSH, kde účinky 5- a10-µM Gomisinu N boli porovnateľné s účinkami 10- a {{12 }} µM PTU, v tomto poradí (obrázok 1C). Bunky NHEM ošetrené Gomisinom N vykazovali znížené hladiny L-DOPA, čo naznačuje, že GomisinN inhibujetyrozinázaaktivita v kultivovaných bunkách (obrázok 1E). Tieto zistenia nás viedli k ďalšiemu skúmaniu základného mechanizmu, ktorým Gomisin N inhibuje melanogenézu.
Skúmali sme, čiGomisin Npriamo moduluje katalytickú aktivitutyrozinázain vitro. Na rozdiel od kyseliny kojovej, Gomisin N nevykazoval inhibičné účinky na aktivitu hubovej tyrozinázy (obrázok 2A). Aktivita bunkovej tyrozinázy v lyzátoch melanómových buniek B16 však bola významne znížená pomocou Gomisínu N s ošetrením -MSH aj bez neho (obrázok 2B, C). Zistilo sa, že inhibícia bunkovej tyrozinázovej aktivity Gomisinu N po stimule -MSH je významnejšia ako inhibícia pozitívnej kontroly kyseliny kojovej (obrázok 2C).
Predpokladali sme, že anti-melanogénna funkcia Gomisinu N sa môže vyskytnúť prostredníctvom transkripčnej alebo post-transkripčnej regulácie tyrozinázy a proteínov súvisiacich s tyrozinázou (TRP). Aby sme to potvrdili, zmerali sme hladiny expresie signálnych molekúl v dráhe MC1R, ktorá je hlavným determinantom kvantita a kvalita produkcie melanínu v melanocytoch. Očakávalo sa, že sme pozorovali, že Gomisin N znížil hladiny MC1R a adenylylcykláz 2 v bunkách Melan-A (obrázok 3A–C). ďalejGomisin Nznížila expresiu MITF a jeho cieľových proteínov vrátane tyrozinázy, TRP-1 a TRP{1}} (obrázok 3A,D–G). Tieto výsledky naznačujú, že znížené hladiny obsahu melanínu po liečbe Gomisinom N sú výsledkom deaktivácie dráhy MC1R.
Na druhej strane dráhy PI3K/Akt a MAPK/ERK môžu fosforylovať MITF, a tým môžu post-transkripčne modulovať jeho aktivitu [45]. Avšak celkový účinok aktivácie dráh PI3K/Akt a MAPK/ERK vmelanogenézaje kontroverzný. Dráhy PI3K/Akt aj MAPK/ERK sú v ľudských melanómoch konštitutívne aktivované v dôsledku nahromadených mutácií [46]. Je známe, že depigmentácia v Mel-Ab bunkách sprostredkovaná C2-ceramidom sa vyskytuje prostredníctvom zníženia hladín p-Akt [47]. Existuje niekoľko prírodných zlúčenín, ktoré aktivujú melanogenézu zvýšením hladiny p-ERK v bunkách melanómu B16 [28]. Na rozdiel od toho existuje tiež dôkaz, že zvýšené hladiny p-ERK a p-Akt inhibujú syntézu melanínu [28,48]. Komplexnú inreguláciu melanogenézy možno čiastočne vysvetliť skutočnosťou, že fosforylácia zvyšuje transkripčnú aktivitu MITF, ale súčasne indukuje degradáciu MITF závislú od ubiquition-proteozómu [26,49–51]. Naše údaje ukázali, že hladiny p-Akt aj p-ERK boli upregulované v bunkách Melan-A ošetrených Gomisínom N (obrázok 3H–J). To znamená, že dráhy PI3K/Akt a MAPK/ERK môžu prispievať k inhibícii produkcie melanínu.
Ďalej sme potvrdili antimelanogénnu aktivitu Gomisinu N v modeli zebrafish in vivo. Embryá zebričky ošetrené Gomisinom N vykazovali významné zníženie pigmentácie melanínu (obrázok 4). Okrem toho Gomisin N výrazne znížil hladinytyrozináza, MITF, TRP-1 a TRP-2 pri vývoji embryí zebričky. Tieto zistenia to spoločne naznačujúGomisin Nindukuje depigmentáciu znížením expresie MITF a melanogénnych enzýmov in vivo. Antimelanogénna aktivita Gomisinu N bola ďalej potvrdená v bunkách ľudského melanómu MNT-1 stimulovaných rapamycínom. Hoci Gomisin N viedol len k malým zmenám v obsahu melanínu v MNT-1 bunkách (obrázok 1D), bol účinný na zvrátenie rapamycínom indukovanej upregulácie MITF, TRP-1 a TRP-2 v spôsobom závislým od koncentrácie (obrázok 6A, C–E). Celkovo vzaté, regulačný účinokGomisin Nna MITF a melanogénnych enzýmoch bol reprodukovateľne nájdený v myších a ľudských bunkách, ako aj v embryách zebričiek.
Aby sme to zhrnuli, táto práca naznačuje, že Gomisin N môže mať vysoký potenciál ako románbielenie pokožkyagent. Zdá sa, že Gomisin N inhibujemelanogenézapotlačením expresie MITF prostredníctvom dráhy MC1R namiesto priamej modulácie katalytickej aktivitytyrozinázaa TRP. Aj keď je potrebné ešte objasniť podrobné mechanizmy, depigmentácia vyvolaná Gomisinom N bude pravdepodobne spojená s aktiváciou dráh PI3K/Akt a MAPK/ERK (obrázok 7).

4. Materiály a metódy
4.1. Materiály
RPMI1640 bol zakúpený od Gibco-BRL (Gaithersburg, MD, USA). Dulbeccovo modifikované Eaglovo médium (DMEM), fetálne bovinné sérum (FBS) a penicilín-streptomycín (PS) boli zakúpené od Hyclone (Carlsbad, CA, USA). Médium na rast melanocytov bolo zakúpené od PromoCell (Heidelberg, Nemecko). Fenylmetylsulfonylfluorid (PMSF), 12-O-tetradekanoylforbol-13-acetát (TPA), kyselina kojová, 1-fenyl-2-tiomočovina (PTU), hubová tyrozináza, 3,{{ 9}}dihydroxy-1-fenylalanín (L-DOPA), -MSH, dimetylsulfoxid (DMSO) a paraformaldehyd boli zakúpené od SigmaChemical Co. (St. Louis, MO, USA).Gomisin Nzlúčeninu poskytla Chul Young Kim (Hanyang University, Ansan, Kórea). Rapamycín bol zakúpený od Sigma-Aldrich (St. Louis, MO, USA).
4.2. Bunková kultúra
Bunková línia myšieho melanómu B16F10 bola poskytnutá z Korean Cell Line Bank (Seoul, Kórea). Bunky myšacieho melanocytu Melan-A [52] boli veľkorysým darom od Dr. Byeong Gon Lee (SkinResearch Institute, Amore Pacific Co., Yongin -si, Kórea). Bunky ľudského MNT-1 melanómu štedro poskytla Aeyeong Lee (koláž medicíny na univerzite Dongguk, Goyang-si, Kórea). Primárne normálne ľudské epidermálne melanocyty (NHEM) boli zakúpené od PromoCell (Heidelberg, Nemecko). Bunky Melan-A sa pestovali v médiu RPMI 1640 (Gibco, Carlsbad, CA, USA) doplnenom 10 percentami FBS, 1 percentami PS a 200 nM TPA. DMEM doplnený 10 percentami FBS a 1 percentom PS sa použil na udržiavanie buniek Melan-A a buniek NHEM. Všetky bunky boli inkubované pri 37 °C v inkubátore s 5 % CO2.
4.3. Meranie obsahu melanínu
Bunky Melan-A sa vysiali na 24-jamkovú doštičku (1 x 105 buniek/jamku) a ošetriliGomisin Na potom inkubovať 72 hodín. Po 72 hodinách sa zmeral obsah melanínu, ako bolo opísané vyššie [53]. Stručne, po odstránení kultivačného média sa bunky trikrát premyli PBS. Potom sa do každej jamky pridal roztok hydroxidu sodného (1 ml, 1 N), aby sa rozpustil melanín. Absorbancia pri 405 nm sa merala pomocou čítačky mikrodoštičiek. Tento test sa opakoval s bunkami B16F10 (2 x 104 buniek/jamka) a MNT{10}} bunkami podľa rovnakej metódy.
4.4. Western Blot analýza
Bunky Melan-A sa vysiali do 100 mm misiek (1 x 106 buniek/misku) a ošetrili 1, 5 alebo 10 uMGomisin Npočas troch dní pri 37 ◦C. Bunky boli premyté PBS a potom zozbierané pomocou škrabky. Oddelené bunky boli vložené do 1 ml PBS a centrifugované pri 7500 rpm počas 5 minút. Po odstránení horného roztoku boli bunkové pelety lyzované lyzačným pufrom (50 mM Tris-HCI, pH 8.{15}}, 0,1 percenta SDS, 150 mM NaCl, 1 percenta NP-40, 0,02 % azidu sodného, 0,5 % deoxycholátu sodného, 100 ug/ml PMSF, 1 g/ml aprotinínu) počas 24 hodín pri 4 °C. Celkové proteíny boli extrahované pomocou ultracentrifúgy pri 12, 000 rpm počas 30 minút pri 4 °C. Obsah proteínu sa meral pomocou Bradfordovho testu. Proteíny (30 ug) sa oddelili pomocou gélu elektroforézy na 10 percentnom dodecylsulfátovom polyakrylamidovom géli (SDS-PAGE) a preniesli sa na anitrocelulózovú membránu. Membrána bola blokovaná 1 hodinu 5 percentným odstredeným mliekom v Tris-pufrovanom fyziologickom roztoku s Tween-20 (TBST) a potom inkubovaná 12 hodín pri 4 °C s primárnymi protilátkami zameranými na -tubulín (Santa Cruz, CA, USA ), MITF (bunková signalizácia, Danvers, MA, USA), tyrozináza (bunková signalizácia), ERK (bunková signalizácia), fosfo-ERK (bunková signalizácia), AKT (bunková signalizácia), fosfo-AKT (bunková signalizácia), MC1R ( Santa Cruz), adenylylcyklázy 2 (Santa Cruz), TRP-1 (Santa Cruz) a TRP-2 (Santa Cruz). Po odstránení primárnych protilátok boli membrány trikrát premyté TBST a inkubované so sekundárnym protilátky (králičí anti-kozí IgG-HRP; myšací anti-králičí HRP, Santa Cruz) počas 1 h. Membrány boli ošetrené zosilneným chemiluminiscenčným činidlom s použitím zobrazovacieho systému ChemiDoc XRS plus (Bio-Rad, Hercules, CA, USA). Denzitometrická analýza pásov sa uskutočnila pomocou softvéru Image MasterTM 2D Elite (verzia 3.1, GE Healthcare, Chicago, IL, USA).
4.5. Test tyrozinázovej aktivity
Odhadnúť inhibičný účinok Gomisinu N na hubytyrozinázaaktivity, sa tyrozináza inkubovala s 1, 5 alebo 10 uMGomisin Nalebo pozitívna kontrola kyselina kojová. Každá vzorka bola rozpustená v metanole. L-DOPA (8,3 mM) a hubová tyrozináza (125 U) sa zriedili v 80 mM fosfátovom pufri (pH 6,8). 40 ul každej vzorky a 120 ul L-DOPA sa zmiešalo na 96-jamkovej doštičke, potom sa pridalo 40 ul zriedenej hubovej tyrozinázy. Doštičky sa potom inkubovali 15 minút a merala sa absorbancia pri 490 nm pomocou čítačky mikrodoštičiek.
tyrozinázaaktivita v lyzátoch melanómových buniek B16 sa merala s alebo bez ošetrenia -MSH, ako už bolo opísané v Ohguchi et al. [54] s malými úpravami. Bunkový lyzát bol pripravený tak, ako je opísané vyššie v časti analýzy Western Blot. Celkové proteíny v supernatante sa merali Bradfordovým testom s použitím bovinného sérového albumínu ako štandardu [55]. Rovnaké množstvo proteínov sa zriedilo a použilo na test tyrozinázovej aktivity.

inhibovať aktivitu tyrozinázy
4.6. Farbenie L-DOPA v bunkách NHEM
Bunky NHEM sa naočkovali do {{0}}jamkovej platne a inkubovali sa 72 hodín s Gomisinom N. Bunky sa fixovali 4% paraformaldehydom počas 40 minút, po čom nasledovalo ošetrenie 0,1% Tritonom X{ {6}} počas 2 minút. Do každej jamky sa pridala L-DOPA (0,1 percenta), nasledovala inkubácia počas 2 hodín. Po odstránení roztoku sa bunky dvakrát premyli PBS. Obrázky boli odfotografované mikroskopom.
4.7. Pokusy so zebričkou
Embryá zebrafish boli získané od Zebrafish Resource Bank (Daegu, Kórea). Embryá boli ošetrené Gomisinom N počas 72 hodín. Depigmentačný účinokGomisin Nna embryách zebričiek bol pozorovaný pod stereomikroskopom. Na analýzu Western blot sa embryá ošetrené Gomisinom N lýzovali použitím lyzačného pufra, z ktorého sa pripravili celkové proteíny, ako je uvedené vyššie.
5. Závery
Náš výsledok podporuje názor, že Gomisin N má vysoký potenciál na použitie ako funkčná potravinabielenie pokožkyagent.Gomisin Nje jednou z hlavných lignanových zlúčenín v S. Chinensis. V skutočnosti, S. Chinensis je bylinný liek používaný na liečbu mnohých ľudských chorôb. Na preukázanie bezpečnosti Gomisinu N na koži sú však potrebné ďalšie epidemiologické štúdie. V dôsledku toho in vivo štúdie a klinické štúdie budú môcť jasnejšie preukázať účinnosť GomisinN. Na záver, táto štúdia to naznačujeGomisin Nmôže byť potenciálnym hypopigmentovým činidlom a prirodzenýmbielenie pokožkykandidát pre kozmetický priemysel.

cistanche zlepšujú bielenie
Referencie
1. Alaluf, S.; Atkins, D.; Barrett, K.; Blount, M.; Carter, N.; Heath, A. Vplyv epidermálneho melanínu na objektívne merania farby ľudskej pokožky. Pigment Cell Res. 2002, 15, 119–126. [CrossRef] [PubMed]
2. D'Mello, SA; Finlay, GJ; Baguley, BC; Askarian-Amiri, ME signálne dráhy v melanogenéze. Int. J.Mol. Sci. 2016, 17, 1144. [CrossRef] [PubMed]
3. Slominski, A.; Tobin, DJ; Shibahara, S.; Wortsman, J. Pigmentácia melanínu v koži cicavcov a jej hormonálna regulácia. Physiol. Rev. 2004, 84, 1155–1228. [CrossRef] [PubMed]
4. Herrling, T.; Jung, K.; Fuchs, J. Úloha melanínu ako ochrancu pred voľnými radikálmi v koži a jeho úloha ako indikátora voľných radikálov vo vlasoch. Spectrochim Acta A Mol. Biomol. Spectrosc. 2008, 69, 1429–1435. [CrossRef] [PubMed]
5. Brozyna, AA; Jozwicki, W.; Roszkowski, K.; Filipiak, J.; Slominski, AT Obsah melanínu v melanomametastázach ovplyvňuje výsledok rádioterapie. Oncotarget 2016, 7, 17844–17853. [CrossRef] [PubMed]
6. Slominski, A.; Wortsman, J.; Plonka, PM; Schallreuter, KU; Paus, R.; Tobin, DJ Pigmentácia vlasových folikulov.J. Vyšetrovať. Dermatol. 2005, 124, 13-21. [CrossRef] [PubMed]
7. Slominski, A.; Zmijewski, MA; Pawelek, J. L-tyrozín a L-dihydroxyfenylalanín ako hormónom podobné regulátory funkcií melanocytov. Pigment Cell Melanoma Res. 2012, 25, 14–27. [CrossRef] [PubMed]
8. Lee, AY Nedávny pokrok v patogenéze melazmy. Pigment Cell Melanoma Res. 2015, 28, 648–660. [CrossRef][PubMed]9. Speckaert, R.; van Gele, M.; Speckaert, MM; Lambert, J.; van Geel, N. Biológia hyperpigmentačných syndrómov. Pigment Cell Melanoma Res. 2014, 27, 512–524. [CrossRef] [PubMed]
10. Slominski, RM; Zmijewski, MA; Slominski, AT Úloha melanínového pigmentu pri melanóme. Exp. Dermatol.2015, 24, 258–259. [CrossRef] [PubMed]11. Slominski, A.; Wortsman, J.; Tobin, DJ Kožný serotonínergný/melatonínergný systém: Zabezpečenie miesta pod slnkom. FASEB J. 2005, 19, 176–194. [CrossRef] [PubMed]
12. Sarkar, R.; Arora, P.; Garg, KV Cosmeceuticals pre hyperpigmentáciu: Čo je k dispozícii? J. CutaneousAesthet. Surg. 2013, 6, 4–11. [CrossRef] [PubMed]
13. Miyamura, Y.; Coelho, SG; Wolber, R.; Miller, SA; Wakamatsu, K.; Zmudzka, BZ; Ito, S.; Smuda, C.; Passeron, T.; Choi, W.; a kol. Regulácia pigmentácie ľudskej kože a reakcie na ultrafialové žiarenie. Pigment Cell Res. 2007, 20, 2–13. [CrossRef] [PubMed]
14. Davis, EC; Callender, VD Pozápalová hyperpigmentácia: Prehľad epidemiológie, klinických vlastností a možností liečby vo farbe pleti. J. Clin. Estét. Dermatol. 2010, 3, 20-31. [PubMed]
15. Sales-Campos, H.; Souza, PR; Peghini, BC; da Silva, JS; Cardoso, ČR Prehľad modulačných účinkov kyseliny olejovej na zdravie a chorobu. Mini. Med. Chem. 2013, 13, 201–210. [CrossRef] [PubMed]
16. Parvez, S.; Kang, M.; Chung, HS; Cho, C.; Hong, MC; Shin, MK; Bae, H. Prehľad a mechanizmus činidiel na depigmentáciu a zosvetľovanie pokožky. Phytother. Res. 2006, 20, 921-934. [CrossRef] [PubMed]
17. Luo, L.; Jiang, L.; Geng, C.; Cao, J.; Zhong, L. Hydrochinónom indukovaná genotoxicita a oxidačné poškodenie DNA v bunkách HepG2. Chem. Biol. Interagujte. 2008, 173, 1–8. [CrossRef] [PubMed]
18. Enguita, FJ; Leitao, AL Hydrochinón: Znečistenie životného prostredia, toxicita a mikrobiálne odpovede. BioMed Res. Int. 2013, 2013, 542168. [CrossRef] [PubMed]
19. Draelos, ZD Prípravky na zosvetlenie pokožky a kontroverzia hydrochinónu. Dermatol. Ther. 2007, 20,308-313. [CrossRef] [PubMed]
20. Koo, JH; Lee, I.; Yun, SK; Kim, HU; Park, BH; Zmydelnený pupalkový olej Park, JW znižuje melanogenézu v bunkách melanómu B16 a znižuje pigmentáciu kože spôsobenú UV žiarením u ľudí. Lipidy 2010,45, 401–407. [CrossRef] [PubMed]
21. Cordell, GA; Colvard, MD Prírodné produkty a tradičná medicína: Zapnutie paradigmy. J. Nat. Prod.2012, 75, 514–525. [CrossRef] [PubMed]
22. Panossian, A.; Wikman, G. Farmakológia Schisandry Chinensis Bail: Prehľad ruského výskumu a použitia v medicíne. J. Ethnopharmacol. 2008, 118, 183–212. [CrossRef] [PubMed]
23. Chen, P.; Pang, S.; Yang, N.; Meng, H.; Liu, J.; Zhou, N.; Zhang, M.; Xu, Z.; Gao, W.; Chen, B.; a kol. Priaznivé účinky schizandrínu B na srdcovú funkciu v myšom modeli infarktu myokardu. PLoS ONE 2013, 8,e79418. [CrossRef] [PubMed]
24. Lee, HJ; Jo, S.; Ryu, J.; Jeong, HS; Lee, G.; Ryu, MH; Jung, MH; Kim, H.; Kim, BJ Účinky SchisandraChinensis Turcz. ovocie pri kontaktnej dermatitíde vyvolanej dinitrofluórbenzénom u myší. Mol. Med. Správa 2015,12, 2135–2139. [CrossRef] [PubMed]
25. Chun, JN; Cho, M.; Takže ja.; Jeon, JH Ochranné účinky extraktu z ovocia Schisandra Chinensis a jeho lignanov proti kardiovaskulárnym ochoreniam: Prehľad molekulárnych mechanizmov. Fitoterapia 2014, 97, 224–233.[CrossRef] [PubMed]
26. Kang, OH; Chae, HS; Choi, JH; Choi, HJ; Park, PS; Cho, SH; Lee, GH; Takže, HY; Choo, YK; Kweon, OH; a kol. Účinky vodného extraktu Schisandra Fructus na uvoľňovanie cytokínov z bunkovej línie ľudského žíru. J. Med. Jedlo 2006, 9, 480–486. [CrossRef] [PubMed]
27. Poma, A.; Bianchini, S.; Miranda, M. Inhibícia produkcie mikrojadier indukovanej L-tyrozínom fenyltiomočovinou v bunkách ľudského melanómu. Mutat. Res. 1999, 446, 143–148. [CrossRef]
28. Kim, HJ; Kim, IS; Dong, Y.; Lee, IS; Kim, JS; Kim, JS; Woo, JT; Cha, Efekt cirsimaritínu indukujúci melanogenézu prostredníctvom zvýšenia transkripčného faktora spojeného s mikroftalmiou a expresie tyrozinázy. Int. J. Mol. Sci. 2015, 16, 8772–8788. [CrossRef] [PubMed]
29. Busca, R.; Abbe, P.; Mantoux, F.; Aberdam, E.; Peyssonnaux, C.; Eychene, A.; Ortonne, JP; Ballotti, R. Rassprostredkuje cAMP-dependentnú aktiváciu extracelulárnych signálom regulovaných kináz (ERK) v melanocytoch. EMBO J. 2000, 19, 2900–2910. [CrossRef] [PubMed]
30. Busca, R.; Ballotti, R. Cyklický AMP kľúčový posol v regulácii pigmentácie kože. Pigment Cell Res. 2000, 13, 60–69. [CrossRef] [PubMed]
31. Hah, YS; Cho, HY; Lim, TY; Park, DH; Kim, HM; Yoon, J.; Kim, JG; Kim, CY; Yoon, TJ Indukcia melanogenézy rapamycínom v bunkách ľudského MNT-1 melanómu. Ann. Dermatol. 2012, 24, 151–157. [CrossRef][PubMed]
32. Yun, WJ; Kim, EY; Park, JE; Jo, SY; Bang, SH; Chang, EJ; Chang, SE Proteínový ľahký reťazec 3 spojený s mikrotubulami sa podieľa na melanogenéze prostredníctvom regulácie expresie MITF v melanocytoch. Sci. Správa. 2016, 6, 19914. [CrossRef] [PubMed]
33. Spritz, RA; Sluch, VJ, Jr. Genetické poruchy pigmentácie. Adv. Hum. Genet. 1994, 22, 1-45. [PubMed]
34. Kadekaro, AL; Chen, J.; Yang, J.; Chen, S.; Jameson, J.; Swope, VB; Cheng, T.; Kadakia, M.; Abdel-Malek, Z. - hormón stimulujúci melanocyty potláča oxidačný stres prostredníctvom a53-sprostredkovanej signálnej dráhy v ľudských melanocytoch. Mol. Cancer Res. 2012, 10, 778–786. [CrossRef] [PubMed]
35. Wasmeier, C.; Hume, AN; Bolasco, G.; Seabra, MC Melanosomes v skratke. J. Cell Sci. 2008, 121,3995-3999. [CrossRef] [PubMed]
36. Brozyna, AA; Jozwicki, W.; Carlson, JA; Slominski, AT Melanogenéza ovplyvňuje celkové prežitie a prežitie bez ochorenia u pacientov s melanómom štádia III a IV. Hum. Pathol. 2013, 44, 2071–2074. [CrossRef] [PubMed]
37. Slominski, A.; Kim, TK; Brozyna, AA; Janjetovič, Z.; Brooks, DL; Schwab, LP; Skobowiat, C.; Jozwicki, W.; Seagroves, TN Úloha melanogenézy v regulácii správania melanómu: Melanogenéza vedie k stimulácii expresie HIF{1}} a sprievodných dráh závislých od HIF. Arch. Biochem. Biophys. 2014, 563,79–93. [CrossRef] [PubMed]
38. Kim, HJ; Lee, JH; Shin, MK; Hyun Leem, K.; Kim, YJ; Lee, MH Inhibičný účinok extraktu Gastrodia elata na melanogenézu v bunkách melanómu HM3KO. J. Cosmet. Sci. 2013, 64, 89–98. [PubMed]
39. Hemesath, TJ; Cena, ER; Takemoto, C.; Badalian, T.; Fisher, DE MAP kináza spája transkripčný faktor Mikroftalmia so signalizáciou c-Kit v melanocytoch. Príroda 1998, 391, 298–301. [PubMed]
40. Cena, ER; Ding, HF; Badalian, T.; Bhattacharya, S.; Takemoto, C.; Yao, TP; Hemesath, TJ; Fisher, DELlineage-špecifická signalizácia v melanocytoch. Stimulácia C-kitu privádza p300/CBP do mikroftalmie.J. Biol. Chem. 1998, 273, 17983–17986. [CrossRef] [PubMed]
41. Bertolotto, C.; Abbe, P.; Hemesath, TJ; Bille, K.; Fisher, DE; Ortonne, JP; Ballotti, R. Produkt Microphthalmiagene ako signálny prevodník v cAMP-indukovanej diferenciácii melanocytov. J. Cell Biol. 1998, 142,827-835. [CrossRef] [PubMed]
42. Pogenberg, V.; Ogmundsdottir, MH; Bergsteinsdottir, K.; Schepsky, A.; Phung, B.; Deineko, V.; Milewski, M.;Steingrimsson, E.; Wilmanns, M. Obmedzená dimerizácia leucínového zipsu a špecifickosť rozpoznávania DNA hlavného regulátora melanocytov MITF. Genes Dev. 2012, 26, 2647–2658. [CrossRef] [PubMed]
43. Flaherty, KT; Hodi, FS; Fisher, DE Od génov k liekom: Cielené stratégie pre melanóm. Nat. Rak 2012, 12, 349–361. [CrossRef] [PubMed]
44. Lee, TH; Seo, JO; Baek, SH; Kim, SY Inhibičné účinky resveratrolu na syntézu melanínu v ultrafialovej B-indukovanej pigmentácii v koži morčiat. Biomol. Ther. 2014, 22, 35–40. [CrossRef] [PubMed]
45. Su, TR; Lin, JJ; Tsai, CC; Huang, TK; Yang, ZY; Wu, MO; Zheng, YQ; Su, CC; Wu, YJ Inhibícia melanogenézy kyselinou galovou: Možné zapojenie signálnych dráh PI3K/Akt, MEK/ERK a Wnt/-katenín v bunkách B16F10. Int. J. Mol. Sci. 2013, 14, 20443–20458. [CrossRef] [PubMed]
46. Yajima, I.; Kumasaka, MY; Thang, ND; Goto, Y.; Takeda, K.; Yamashita, O.; Iida, M.; Ohgami, N.; Tamura, H.; Kawamoto, Y.; a kol. Signalizácia RAS/RAF/MEK/ERK a PI3K/PTEN/AKT pri progresii a terapii malígneho melanómu. Dermatol. Res. Prax. 2012, 2012, 354191. [CrossRef] [PubMed]
47. Kim, DS; Kim, SY; Mesiac, SJ; Chung, JH; Kim, KH; Cho, KH; Park, KC Ceramid inhibuje proliferáciu buniek prostredníctvom inaktivácie AKT/PKB a znižuje syntézu melanínu v bunkách Mel-Ab. Pigment Cell Res. 2001, 14, 110-115. [CrossRef] [PubMed]
48. Kim, JH; Baek, SH; Kim, DH; Choi, TY; Yoon, TJ; Hwang, JS; Kim, MR; Kwon, HJ; Lee, CHDregulácia syntézy melanínu pomocou A a jej aplikácia na model blesku in vivo. J.Investig. Dermatol. 2008, 128, 1227–1235. [CrossRef] [PubMed]
49. Hartman, ML; Czyz, M. MITF v melanóme: Mechanizmy za jeho prejavom a aktivitou. Cell Mol.Life Sci. 2015, 72, 1249–1260. [CrossRef] [PubMed]
50. Kim, DS; Hwang, ES; Lee, JE; Kim, SY; Kwon, SB; Park, KC sfingozín-1-fosfát znižuje syntézu melanínu prostredníctvom trvalej aktivácie ERK a následnej degradácie MITF. J. Cell Sci. 2003, 116,1699–1706. [CrossRef] [PubMed]
51. Xu, W.; Gong, L.; Haddad, MM; Bischof, O.; Campisi, J.; Áno, ET; Medrano, EE Regulácia hladín proteínu MITF transkripčného faktora spojeného s mikroftalmiou asociáciou s enzýmom hUBC9 konjugujúcim ubikvitín. Exp. Cell Res. 2000, 255, 135–143. [CrossRef] [PubMed]
52. Bennett, DC; Cooper, PJ; Hart, IR Línia netumorogénnych myších melanocytov, syngénnych s melanómom B16 a vyžadujúcich pre rast nádorový promótor. Int. J. Cancer 1987, 39, 414-418. [CrossRef][PubMed]
53. Meira, WV; Heinrich, TA; Cadena, SM; Martinez, GR Melanogenéza inhibuje dýchanie v bunkách melanómu B16-F10, pričom zvyšuje obsah mitochondriálnych buniek. Exp. Cell Res. 2017, 350, 62–72. [CrossRef][PubMed]
54. Ohguchi, K.; Tanaka, T.; Iliya, I.; Ito, T.; Iinuma, M.; Matsumoto, K.; Akao, Y.; Nozawa, Y. Gnetol ako inhibítor potentyrozinázy z rodu Gnetum. Biosci. Biotechnol. Biochem. 2003, 67, 663-665. [CrossRef] [PubMed]
55. Uchida, R.; Ishikawa, S.; Tomoda, H. Inhibícia tyrozinázovej aktivity a melanínovej pigmentácie 2-hydroxytyrozolom. Acta Pharm. Sinica B 2014, 4, 141–145. [CrossRef] [PubMed]
