Naratívna recenzia o storočí respiračných pandémií od španielskeho fu po COVID-19 a vplyv nanotechnológií na diagnostiku COVID-19 a posilnenie imunitného systému
Jun 09, 2023
Úvod
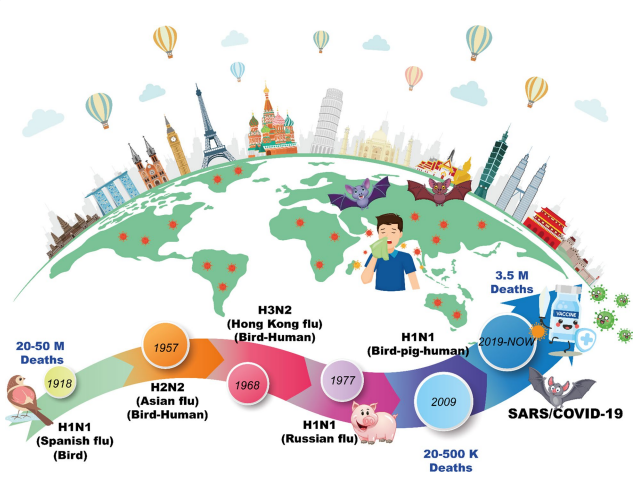
Rýchle šírenie v rámci existujúcich vysokonákazlivý závažný akútny respiračný syndróm-2(SARS-2) alebo takzvaný Coronavirus 2019 (COVID-19)choroby, nám pripomenuli ďalšie pandémie, ktoré sa staliv minulom storočí (H1N1 španielske fu) a pokračovalv súčasnom storočí (SARS, MERS a COVID-19) [1–3]. Po sérii respiračných vírusových pandémiíchoroby, ktoré sa začali v rokoch 1918–1919 záhadnýma smrteľné ochorenie nazývané H1N1 španielska chrípka a niektorévedci to nazvali matka pandémií [4], kvôlitáto pandémia infikovala viac ako tretinu z nichsvetovej populácie a vyžiadal si približne 50 miliónovživotov s netypicky extrémnymi klinickými príznakmiu mladých dospelých, predtým bez chorôb, pandémiebola hlavnou príčinou smrti [5]. v tejto súvislostiSARS-CoV-2 a vírusy chrípky A/H1N1 z roku 1918 majúniektoré spoločné vlastnosti, napríklad sú podobnézákladné reprodukčné čísla (R0), ktoré sa líšia od 2 do 4,a podobné vzorce vylučovania od infekčných pacientov,a teda pravdepodobne budú mať podobné generačné rozdiely. V tandeme, COVID-19 môže mať obdobie latencie podobné akochrípka [6]. Potom, v súčasnom tisícročí,svet bol svedkom pretrvávajúcich vírusových útokov znová vírusová rodina nazývaná Coronaviruses (CoV) [7]. CoV, obsahujúce podrodinu ortokoronavírusov apodčeľaď Torovirinae. Te Orthocoronavirinae subrodina zahŕňa štyri rody: alfa koronavírus,beta koronavírus, gama koronavírus adelta koronavírus [8]. Beta koronavírusy rodov encomprejsť na závažný akútny respiračný syndróm (SARS),Middle-East-Respiratory-Syndrome (MERS), ľudskýCoV-229E (HCoV-229E), HCoV-OC43 a CoronaVírus-2019 (COVID-19) [3].
V rokoch 2002, 2012 a 2019 svet napadli trajavírusové ochorenia dýchacích ciest SARS, MERS, aCOVID-19. Koronavírusy sú obalené,nesegmentovaná, pozitívna, jednovláknová RNAvírusy, ktoré vykazujú charakteristický vzhľad pod negelektrónová mikroskopia s aktívnym farbením [9].

Cistanche štandardizovaný extrakt na zlepšenie imunitného systému
Informovala o tom WHO na juhu Čínyprovincia Guangdong, november 2002, bez aktualizáciebola prijatá od vlády Číny až dokoncom marca, obrovských 792 prípadov a 31 úmrtíboli nahlásené. Informovalo o tom čínske ministerstvo zdravotníctvaviac ako 8,000 prípadov. Odhaduje sa, že tam boli1 tisíc prípadov chorôb a asi 774 úmrtí, dávaťmiera úmrtnosti asi 7 percent. Zásobník hostiteľainfekcia sa považuje za ázijskú cibetku (Pagumalarvata). Očakávalo sa, že trans z hostiteľa na človekamisijné miesta by boli otvorené trhy, ako je to v prípadeaktuálne prepuknutie ochorenia COVID{0}}. [10]. Globálny SARSepidémia bola úspešne zvládnutá v júli 2003 a čprípady SARS boli hlásené od roku 2004. [11]. Thepo vzniku SARS nasledoval MERS ako druhýnajvýznamnejší koronavírus, ktorý spôsobuje celosvetovú verejnosťzdravotná pohotovosť. Prvýkrát sa objavil v Saudskej Arábii (KSA)v roku 2012, keď pacient vo veku 60 rokov s ťažkým zápalom pľúc[10]. Epidémia vírusu sa prejavila až v r2014, s celkovým počtom zistených prípadov 662 a prípadomindex úmrtnosti 32,97 percenta . Od roku 2014 do roku 2016 1364 prípadovboli pozorované v KSA [10]. Celkovo má 27 krajínbol zasiahnutý MERS počas epidémií v Ázii,Európa, Stredný východ a Severná Amerika. [12]. Theprípady identifikované mimo Blízkeho východu, vrátaneJuhokórejská (SK) epidémia, v ktorej má 186 ľudízistilo sa, že je infikovaný v dôsledku super šíreniaing, zapojili príjemcov transplantátu, ktorí už tak urobiliboli infikovaní na Blízkom východe. Od roku 2012 celkomBolo hlásených 2494 laboratórne potvrdených prípadov MERS,s 858 súvisiacimi úmrtiami (pomer úmrtnosti 34,4 percenta)[10].
V súvislosti s ochorením COVID-19 upozornila WHO na rizikoúroveň krízy CoV na „veľmi vysokú“ 28. februára 2020.11. marca ako incidenty COVID-19 mimo Čínyzvýšil 13-násobne a počet infikovanýchkrajín sa trojnásobne zvýšil na viac ako 118,000 registrovanýchprípadov v 114 rôznych krajinách, pričom viac ako4, 000 úmrtí, WHO vyhlásila COVID-19 za globálnypandemický. Vlády po celom svete pracujúzaviesť protiopatrenia na zadržanie potenciálneškodlivé účinky. Koordinujú sa zdravotnícke organizácietok informácií a vydávanie smerníc k najlepšímminimalizovať dopad hrozby pandémie. medzitýmvýskumníci z celého sveta intenzívne pracujúa informácie o prenosových mechanizmoch,klinické spektrum novej diagnózy ochoreniasa rozvíjajú prístupy k prevencii a liečberýchlo. Mnoho neznámych faktorov týkajúcich sa hostiteľa vírusudynamika a postup epidémie zostáva,vrátane načasovania jeho vrcholu [13].
Nanomateriály (NM) majú špecifické vlastnosti, ktoré sújedinečné, čo ich charakterizuje ako výnimočné materiályschopné aplikovať v spektrálnych zariadeniach, senzoroch a technikáchpoužíva sa pri detekcii, liečbe a vírusocheliminácia z prostredia [14]. Hlavná časťaplikáciami NM je predpovedať a liečiť vírusy vzdravotnú starostlivosť a životné prostredie. V tejto recenzii smestručné informácie o niektorých z týchto použití.

Pôvod pandemických respiračných vírusových ochorení
Vtáčia chrípka sa vyznačuje svojou schopnosťoukontaminovať rôzne druhy zvierat vrátane druhovako sú netopiere, vtáky a cicavce. Aj keď úspešnemedzidruhový prenos je zriedkavý, zohráva kľúčovú úlohupri vytváraní nových vektorov pandémie [14]. Inpandémia v rokoch 1918–1919, marec 1918 bol začiatokjarnej vlny. Rozšíril sa po Európe, USA aÁzie počas nasledujúcich šiestich mesiacov. Hoci úrovne chorobyboli vysoké, úmrtnosť na väčšine miest nebolavýrazne vyššia ako zvyčajne. Druhá alebo jesenná vlnasa šíri po celom svete od septembra do novembra1918 a bola veľmi osudná. V mnohých krajinách tretia vlnadošlo začiatkom roku 1919. Doboví pozorovatelia uzavreliz klinických podobností, ktoré videlirovnaké infekčné ochorenie v postupných vlnách [4]. Tetypické boli mierne formy epidémií vo všetkých troch vlnáchchrípky zaznamenanej počas pandémie v roku 1889 aepidémie vtáčej fu a predchádzajúce medzipandemické roky. Inpohľad na to, dokonca aj rýchly postup z nedodržiavaniaprenesená chrípková infekcia až smrteľný zápal pľúc, charakteristickýjesenných a zimných vĺn 1918–1919, bolpozorované v niekoľkých závažných prípadoch v jarnej vlne [4, 15].
Do roku 2003 len 2 CoV, Human CoV 229E (HCoV-229E) a HCoV-OC43 vedú kľudská choroba [16]. Prejavuje sa miernymi príznakmi naprako bežné prechladnutie u dospelých a závažnejšie ochorenie udojčiat, starých ľudí a ľudí s oslabenou imunitou. Innovembra 2002, početné výnimočné prípady „atypickýchzápal pľúc“ z nevysvetliteľných dôvodov boli hlásené vmesto Foshan, provincia Guangdong, v Číne, kdeveľa zdravotníckeho personálu bolo kontaminovaných [17]. Tis bol21. februára 2003 lekár zaviedol do Hongkonguktorí riešili podobné prípady SARS u Číňanovpevniny, čo viedlo k rozšíreniu závažného zápalu pľúcv Hong Kongu a označený WHO ako „závažnýakútny respiračný syndróm“ dňa 15. marca 2003 [18, 19]. Uplynuli mesiace a došlo k niekoľkým incidentom SARSboli identifikované predtým, ako bol identifikovaný SARS-CoV. Novýb-CoV (SARS-CoV) línie B bol potvrdený akopríčinou prípadov zápalu pľúc SARS dňa 22. marca 2003.Pandémia SARS-CoV sa rozšírila do 29 krajína regiónoch. Bolo jasné, že svetové zdravie, media vedecké rozvojové komunity nebolidostatočne pripravený na vznik SARS. [18]. Objavili sa reťazce prenosu z človeka na človekav Kanade, Toronte, čínskom Taipei, Hong Kongu, Číne,Vietnam Singapur a Hanoj. Vyskytla sa epidémia SARSkrátka história a WHO oznámila vinutiezníženie epidémie SARS v júli 2003 [18].

Desať rokov po poslednom príznaku SARS-CoV, v júni2012, muž zomrel v KSA na vážny zápal pľúc a obličiekslabosť [20]. Novoobjavený koronavírus,blízkovýchodný respiračný syndróm – koronavírus(MERS-CoV), bol identifikovaný z jeho spúta [21]. Objavila sa skupina prípadov závažných respiračných ochorenív apríli 2012 v Jordánsku v nemocnici a boli diagnostikovanípri spätnom pohľade ako MERS12 a skupina troch infikovaných MERSv Spojenom kráľovstve boli zistené v septembri2012 MERS-CoV naďalej rastie a expanduje von„arabský polostrov“. V dôsledku cestovania okontaminovaných jedincov; často tieto novo transmitted prípady MERS viedli k získaniu v nemocniciprenos.[22]. V máji 2015 vypukla v rSK spustil jediný navrátilec zo StreduVýchod a zasiahlo šestnásť kliník a 186 prípadov. Od 26apríla 2016 bolo potvrdených 1 728 prípadov MERS, zčo 624 úmrtí v 27 rôznych krajinách [22].
Skupina prípadov zápalu pľúc spojených s nedávno objaveným-koronavírus sa objavil v čínskom Wu-chane v rdecembra 2019. Dňa 12. januára 2020 sa Svet zdraviaOrganizácia (WHO) označila tento koronavírus za novinku roku 2019koronavírus (2019-nCoV) (WHO). Internanálny výbor navrhol pomenovanie novo identifikovaných osôbkoronavírus ako SARS-CoV-2, obe boli nahlásené 11. februára2020. Čínski vedci rýchlo izolovali SARSCoV-2 od pacienta 7. januára 2020. Tey vyšiel vonna sekvenovanie genómu SARS-CoV-2. Od 1. júla2021 bolo potvrdených 91 833 prípadov COVID-19pevninskej Číne vrátane 4 636 úmrtí. Základná reprodukciačíslo „R0“ SARS-CoV-2 bolo posúdenépodľa štúdií približne 2,2 alebo viac (rozsah 1,4–6,5) askupiny prepuknutia rodinnej pneumónie dopĺňajú dôkaz oneustále rastúcu epidémiu COVID{0}} cez človeka na človekaprenos (obr.1) [23]. Podľa SZO (https://covid19.who.int/); globálne k 20:36 SELČ, 14. apríla 2022, majúbolo potvrdených 500 186 525 prípadov COVID-19 vrátane6 190 349 úmrtí, hlásených WHO. Od 18. apríla2022 bolo celkovo podaných 11 307 908 653 dávok vakcíny.spravované.
Zásobník a spôsob prenosu
Je známe, že pochádzajú vírusy chrípky rôznych druhovu voľne žijúcich vodných vtákov. (Obr.2) [24]. Kým človek-prasapodtypy prenosu už boli zobrazené apodložený, priamy prenos medzi vtákmi au ľudí bol menej rozšírený (ako v prípade H9N2a podtypy H5N1), ale v niektorých prípadoch viedla kúmrtia. [25].
Rezervoár čeľade coronaviridae, ktorýpozostáva z beta-koronavírusu zahŕňa tri pandemics nedávno (SARS, MERS, COVID-19). Netopiere sú obrovsképrírodný rezervoár širokého spektra CoV vrátane SARS-CoV podobnýcha vírusy podobné MERS-CoV (obr.2). Sledovanieštudovala sa genómová sekvencia vírusu COVID-19,genóm pre Bat CoV RaTG13 ukázal 96,2 percentacelková identita genómovej série, čo naznačuje CoVnetopier Dokonca aj ľudský SARS-CoV-2 môže mať rovnakého rodičaVek. Naopak, netopiere tu nie sú dostupné na nákupobchod s morskými plodmi. Mimochodom, synchronizáciaproteínových sekvencií a ďalšie fylogenetické štúdiumodhalili podobné zvyšky, prijímač sa našiel v niekoľkýchdruhov, ktoré ponúkali viac možností na striedaniestrední hostitelia; Pre začiatok, korytnačky, pangolín aobčerstvenie [23].
Všetky pandémie respiračných vírusov sú zoonózne prenášané vzduchomRNA vírusy, ktoré sa medzi sebou prenášajú len zriedkapôvodné formy ľudí, ale mohli zmutovať, aby sa z nich stali ľudiaprenos efektívnejší. Časté a schválenétransmission routes droppings (>Priemer 5 mm, lietaniePrenos'<1 m) make contact with the nose with životaschopné vírusy, ústa, oči alebo horné dýchacie cesty a vzduchom prenášanéprenos“, kde sú kvapky (priemer 5 mm).jadrá [27]. Roky 2002 a 2003 boli príkladmi H1N1pandémia chrípky v SARS a 2009.
Funkcia „priamej komunikácie dotykom“ (bezmožnosť znečistených povrchov) a „nepriamy„šírenie dotykom“ (vrátane infikovaných povrchov).šírenie takýchto pandemických potenciálnych vírusovbol kontroverzný. Napriek tomu rôzne správy avyšetrovania uvádzajú, že nepriama komunikáciaprevláda prenos. Prenosová cesta preiné respiračné vírusy, ako aj chrípka, za určitýchpodmienky [26].
Replikácia vírusu SARS-CoV-2
K replikácii vírusu chrípky dochádza na bunkovej úrovnihlavne v epitelových bunkách črevného traktu vvtákov a v epitelových bunkách dýchacieho traktu vľudia a iné cicavce [27]. U ľudí ribonukleoproteíny(vRNP) sa následne prenášajú dojadro chorých buniek, v ktorom dochádza k transkriptom vírusovej RNAa replikuje sa prostredníctvom enzymatickej aktivityvírusový polymerázový komplex pripojený k vRNP [28]. Tereplikácia vírusovej RNA prebieha prostredníctvom pozitívneho medziproduktukomplementárny ribonukleoproteínový komplex [29]. Transkripcia vírusovej RNA vytvára pozitívne vláknamRNA, ktorá je napojená na čiapočku a polyadenylovaná a potomexportované do cytoplazmy, aby boli preložené do vírusových proteínov. [30]. Vírusové novosyntetizované polymerázy (PA,PB1 a PB2) a vírusové NP sa importujú do jadrazvýšiť rýchlosť syntézy vírusovej-RNA, zatiaľ čo vírusovámembránové proteíny HA, NA a M2 sú transportované azabudovaný do plazmatickej membrány [31].

MERS-CoV a SARS-CoV majú špecifické kódovaniemechanizmus, v ktorom sú asi dve tretiny „vírusovýchRNA“ je preložený do dvoch obrovských polyproteínov, zatiaľ čozostávajúci vírusový genóm sa prepíše do jedného hniezdaséria subgenomických mRNA [22]. V oboch pp1a app1ab, polyproteíny kódujú šestnásť neštrukturálnych proteínov. (nsp1–nsp16), ktorý vyvoláva vírusovú replikázukomplex transkriptázy [32]. Polyproteíny sa štiepiaproteázou podobnou papaínu (PLpro; zodpovedajúce nsp3)dve proteázy a Te proteáza, proteáza podobná 3C(3CLpro; zodpovedajúce nsp5). nsps preusporiadať pambrány odvodené z hrubého endoplazmatického retikula(RER) do dvojmembránových vezikúl, v ktorých saprebieha transkripcia a replikácia vírusu. Te exoribonukleázová (ExoN) funkcia nsp14 je jedinečná vlastnosťkoronavírusov, ktorý zabezpečuje nápravukapacita potrebná na udržanie rozsiahleho RNA genómubez hromadenia škodlivých mutácií. MERS-CoVa SARS-CoV prepisujú 9 a 12 subgenómových RNAresp. Tese kóduje štyri štrukturálne proteíny,menovite spike proteín (S), obal (E), nukleokapsid(N), membrána (M) a niekoľko doplnkových proteínov, ktorénezúčastňujú vírusovej replikácie, ale interferujú svrodená imunitná odpoveď hostiteľa alebo ktorej funkcia jeneznáme alebo nepochopené.
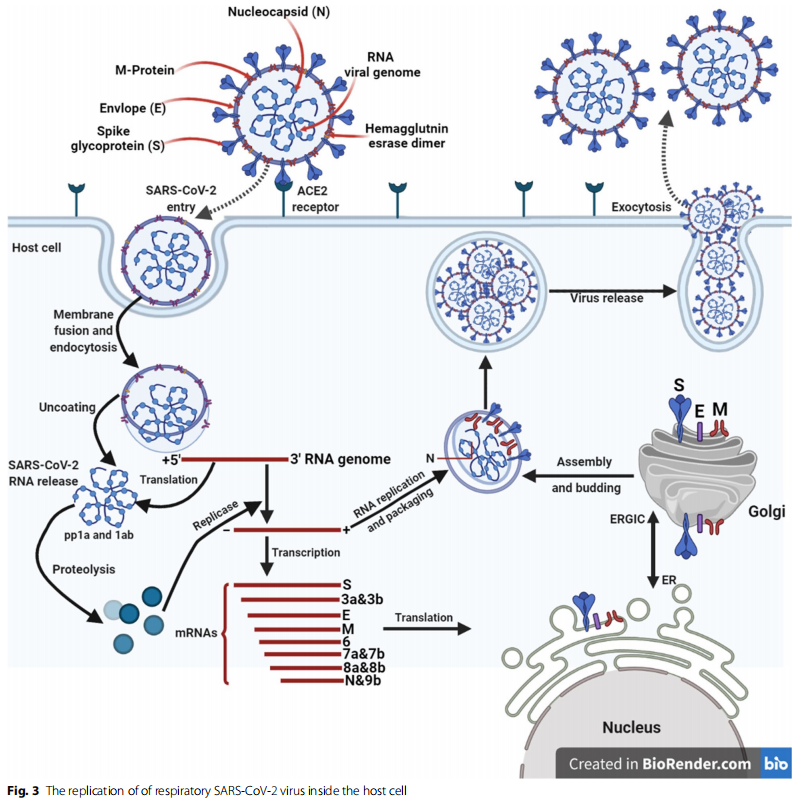
Obalový "E" vrcholový glykoproteín "S" priľne k svojej bunkereceptor, angiotenzín-konvertujúci enzým 2 (ACE2)pre SARS-CoV a dipeptidyl peptidázu 4 (DPP4) preMERS-CoV. "Vírusový RNA genóm" sa dodáva docytoplazme po membránovej fúzii, emisie dok membráne hostiteľskej bunky alebo k endozómovej membráne.Te RNA sa rozbalí, aby sa umožnila translácia týchto dvochpolyproteíny, transkripcia subgenomických RNA areplikácie vírusového genómu. Výsledná obálkaglykoproteíny sa zavádzajú do RER alebo Golgiho membrán; genómová RNA a nukleokapsidové proteínyspolu tvoria nukleokapsidy. Vírusové častice budv ER-Golgiho medzikomorte (ERGIC). Thevezikuly obsahujúce vírus potom fúzujú s plazmatickou membránoudoručiť vírus [22].
Čo sa týka COVID-19 (obr.3), využíva sa genómová RNAako lešenie na priamu transláciu polyproteínu 1a/1ab(pp1a/pp1ab), ktorý kóduje neštrukturálne proteíny(nsps), aby sa vytvoril replikačno-transkripčný komplex(RTC) v dvojmembránových vezikulách (DMV). nakoniecsyntetizuje sa vnorený súbor subgenomických RNA (sgRNA).pomocou RTC v nespojitom režime transkripcie. Tieto subgenomické messengerové RNA (sgRNA)mať spoločné 5′- vodca a 3′- koncové sekvencie. aNásledná akvizícia a ukončenie prepisuvedúcej RNA sa vyskytuje pri regulácii transkripciesekvencie umiestnené medzi otvorenými čítacími rámcami (ORF).Tieto mínus-vláknové gRNA pôsobia ako templát pre subgenomicképrodukciu mRNA.
Typický CoV genóm a subgenómy zahŕňajú atminimálne šesť ORF. Prvé „ORF (ORF1a/b), ktorétvoria asi dve tretiny celkovej dĺžky genómu,kód pre 16 zdriemnutí (nsp1-16), s výnimkou Gammakorona vírus, ktorý nemá nsp1. Existuje a−1 rámposun medzi ORF1a a ORF1b, čo vedie k produkciidvoch polypeptidov: pp1a a pp1ab. Tese polypeptidy sú spracované do 16 zdriemnutí vírusom kódovanýmproteáza podobná chymotrypsínu (3CLpro) alebo hlavná proteáza(Mpro) a jedna alebo dve proteázy podobné papaínu. InéORF na tretine genómu blízko 3′-kódovať hrotaspoň štyri hlavné štrukturálne proteíny: (S), (M), (E) a(N) [33]. Rôzne CoV kódujú špecifické štrukturálne adoplnkové proteíny, ako je HE proteín, 3a/b proteín,a proteín 4a/b, okrem týchto štyroch základnýchštruktúrne proteíny. CoV sgRNA sa používajú na preklad všetkýchštrukturálne a pomocné proteíny [34].
Pre prepnutie hostiteľa je potrebná vírusová adaptáciaa determinanty patogenity
Vírus chrípky A sa zmení na hostiteľa a vytvorí novovyvinutýrodokmeň [35]. Táto infekcia, známa ako zoonotickáponúka možnosť prispôsobiť vírus ďalšiemu hostiteľovi avýsledné pandémie. Keď vstúpi vírus chrípky Atelo, molekula grippe HA (hemaglutinín).okolo vrchu prijíma kyselinu sialovú (N-acetylneuramínovú).hostiteľskej bunky [36]. HA je transmembránový typ glykoproteín ako homotrimér zavedený do vírusového listu.Každý monomér sa skladá z dvoch podjednotiek, HA2 aHA1. V endozómovej oblasti s nízkym pH, štiepená HA s afuzogénna fúzia stonkovej domény HA2 sprostredkúva endozomálnemembrána s vírusovou membránou, ktorá tvorívstup vírusu silný ribonukleoproteín (vRNP) do hostiteľskej bunky[37].
Komplex vRNP pozostáva z 8 jednovláknových,nukleoproteín (NP) vRNA s negatívnym zmyslom a RNA prechrípka-A polymeráza" (zlúčenina PA, PB1 a PB2)[28]. S následnou fúziou môže komplex vRNPsa uvoľní v cytoplazme bunky, po ktorej vstúpijadro úspešným prenosom [37]. To jadroje miesto, kde prebieha syntéza RNA všetkých vírusov chrípkymiesto. Začať proces transkripcie; RNA polymerázavírus sa viaže na vysoko zadržanú a takmer komplementárnu13 na konci 5' jadrovej energie a 12 na konci3'nukleotid" osem segmentov. Napriek tomu polymerázachrípkový vírus nemá žiadnu inherentnú čiapočkovú aktivitu. tosumarizuje, že RNA používajú vírusové masy 5'pre-mRNA hostiteľskej čiapkysager Špeciálny mechanizmus na sprostredkovanie „uchopenia čiapky“.PB1 a PB2 odvodené z bunkového transkripčného proteínu[28]. Neštrukturálny proteín NS1 ovplyvňuje vírusový morfogénesis neskôr v časticiach vírusového replikačného cyklu. všaknie sú to vírusové štrukturálne častice [38].
Identifikácia receptora predstavuje počiatočnú fázuvírusová infekcia hostiteľských buniek a je jednou z najdôležitejšíchfaktory vírusovej infekcie a patogenézy [39]. Zatiaľ čo mnohé iné faktory súvisiace s hostiteľmi a vírusmi môžuovplyvňujú aj účinnosť infekcie a replikácievírusu u konkrétneho hostiteľa, iba tieto faktoryvstupujú do hry, keď je vírus spojený s bunkovou membránouprijímač [40]. Koronavírusy (CoV) majúobalený, jednovláknový RNA genóm, ktorý kóduještyri membránové proteíny, menovite hrot, membrána,obal a nukleokapsidové proteíny, ako je znázornené na obr.3 [2, 41]. S proteíny sú dôležité pre vstup vírusu kono patogenite [42]. Na prahu SARS-CoVlope "E", trimerický S sprostredkuje prienik dovírus do hostiteľských buniek. Najprv sa pripojí k svojmu hostiteľskému prijímaču,enzým konvertujúci angiotenzín 2 (ACE2) anásledne spája hostiteľskú a vírusovú membránu [43]. Daná doména viažuca receptor (RBD) na "S"SARS-CoV je dostatočný na to, aby sa naň naviazal s vysokou afinitouACE2 [44]. Dôležitý prvok v patogenézeSARS-CoV a medzidruhové infekcieidentifikovaná ako väzbová afinita RBD/ACE2 [45]. Theexperimentálna skrížená reaktivita protilátok anti-SARS-CoVs 2019-špičkovými proteínmi nCoV, ktoré by mohli maťvýznamné dôsledky pre rýchlu výrobuprotilátok a vakcín na boj proti 2019-nCoV,je preto naliehavo potrebné [46].
Faktory virulencie pandemických vírusov
Faktory virulencie sa považujú za jeden zo životne dôležitých prvkovktorý hrá významnú úlohu pri adaptácii vírusu nahostiteľská bunka [47]. Pokiaľ ide o pandemickú chrípku, hemaglutinín(HA) je súčasťou povrchového glykoproteínuvírus. s dvoma hlavnými úlohami v najranejšej fázereplikácia vírusu: membránová fúzia a prepojenie receptorov[48]. HA vysokého patogénu vírusu vtáčej chrípky nastavujú anvýznamný príspevok k virulencii. Zvyčajne majúšpecifická sekvencia (tj sekvencia základných aminokyselínv mieste štiepenia, čo napomáha k prevalencii patogenity). [49]. Tento vzor, aj keď sa neodrážav sekvencii HA z roku 1918. Napriek tomu to boloukázali, že ide o vírus s genetickou históriou1918 opakovaná HA pri výrazne zvýšenom titri vpľúc a s veľkým prílivom pľúc z neutrofilova alveolové makrofágy spôsobili vážne poškodenie pľúc. Skutočný vírus z roku 1918 s výraznou chorobnosťou anásledná smrť ukázala podobné výsledky. Tieto výsledkynaznačujú dôležitú úlohu pri chorobe vírusu z roku 1918pre gén HA [50]. Oblasť (oblasti) HA s vysokou virulenciouzatiaľ nebol objavený. Ďalším ústredným faktorom vprepuknutie v roku 1918 je virulencia. Jedna nezvyčajná vlastnosťpandémie v roku 1918 bola taká, akú má mnoho ľudízomrel na vírusovú pneumóniu; vírusové chrípkové vírusy vpľúcny systém infikovaných osôb sa zvyčajne replikujezle a často vedú k život ohrozujúcej vírusovej pneumónii [51]. V pľúcnom systéme infikovaných filamentova primátov (okrem človeka), zaznamenávame efekreplikácie vírusu z roku 1918, ktorý prispel k vírusovejzápal pľúc.
V porovnaní s tým pľúca infikovaných zvierat niemať súčasný ľudský vírus H1N1, aj keď jereprodukované v nosových dutinách. Preto uzatvárameže schopnosť vírusu z roku 1918 expandovať v pľúcach jesúvisí s jeho vysokou ľudskou virulenciou [51]. Poznamenáva sa tiežže vysoké titre vírusu boli založené na génoch NP apolymeráza v pľúcach infikovaných fretiek v roku 1918 [52]. Polymerázové gény sú tiež významné v patogenitea prenos myši u fretiek [53]. Títovýsledky silne zahŕňajú komplex vírusovej RNA polymerázyúspešný prenos vírusu do dolných dýchacích ciesttraktu a uviesť, že v kombinácii s konkrétnymHA, môže stačiť na vyvolanie smrteľného zápalu pľúcpočas pandémie v rokoch 1918–1919 [54]. Patogenitamôže tiež korelovať s inými vírusovými faktormi, ako je naprprípad pandémie NA, NS1, PB1-F2 a ďalších v roku 1918.Proapoptotický vírusový proteín PB1-F2 potrebuje ibaposun v jednej aminokyseline na 66. pozícii na zvýšenievirulencia vírusu v roku 1918 [51]. PB1-F2 z roku 1918expresia podporuje pľúcnu patológiu v primárnomvírusové a sekundárne bakteriálne infekcie [51].
Rešpektovanie beta koronavírusov (SARS, MERS aCOVID-19), obsahujú proteín E pozostávajúci z niekoľkýchaktívne motívy medzi 76 a 109 amino závislými od CoVkyseliny vzhľadom na jeho obmedzenú veľkosť [55]. Modifikácia alebo potlačenieE proteínu v rôznych CoV viedli k vírusoms rôznymi fenotypmi a nezvyčajnými vzájomnými vzťahmimedzi vírusom a hostiteľom vrátane indukcie stresua proteínové reakcie alebo zmeny koncentrácií sbunkový ión kvôli aktivite iónového kanála E proteínu [55, 56]. Všetky tieto praktiky majú dôležitý vplyv napatogenéza CoV. Okrem toho v COVID-19 je „S“.hlavná definícia bunkového tropizmu a preto interspezaisťuje prenos CoV, pretože viaže vírus na bunkureceptora a potom katalyzuje vstup membránovej fúzievírusu [57]. 3D štruktúra elektrónovej mikroskopiez 2019-nCoV vírusu S ukázal svoju podobnosť sS ostatných COV [57]. Ďalšie charakteristikyostatné CoV sa tak môžu odpočítať. Vírus S je transmembránovýtransmembránový proteín typu I s n-koncomštiepiteľný signálny peptid, veľký a vysoko n-glykozylovanýe, transmembránový a cytoplazmatický chvost vložený doklaster zvyškov usporiadaných S [57]. Ektodoména máboli rozdelené do vysoko variabilnej domény S1 medzirody a doménu S2, ktorá je viac konzervovaná akatalyzuje membránovú fúziu. Opera zaväzujúca príjemcuspôsobuje patogenitu [58].
Symptómy a klinické prejavy
Pandemický vírus chrípky H1N1 v rokoch 1918–1919rozdiely v príznakoch a symptómoch podľa mnohýchfaktory, ako je závažnosť prípadov, vek jednotlivca,a sezóna [59]. Prevládalo mierne, nejasné ochoreniev jarných zvestovateľských vlnách zahŕňali symptómyhorných dýchacích ciest, ako je bolesť hrdla, nazofaryngitídaa kašeľ, ako aj systémové prejavyhorúčky, myalgie a vyčerpania (obr.4) [60]. Epistaxabola vykonaná v miernych aj ťažkých prípadoch [61]. Lekár hlási tisíc prípadov v táboreFremont poznamenal, že epistaxa bola bežnou charakteristikoucelej pandémie [60]. Toto sa zvažovalocharakteristickým znakom choroby, pretože krv vždy tečiez nosa a úst pacienta. Trvaniestredne ťažkého ochorenia bola vo všeobecnosti obmedzená na 72 hodín. Typicky, kašeľ nebol produktívny. Prevládala horúčkaaž 104 stupňov F. Niekedy náhla a extrémna prostrácia[62]. Jedna definícia pacienta ako „rýchlo alebo takmernečakane zachvátený pocitom pokorenia, ktorý bolúplne neschopný robiť, čo mohol. Tu bolvýrazné respiračné ťažkosti u pacientov s ťažkým ochorením [62]. Ich symptómy boli pozoruhodne intenzívnecyanóza, hlad vo vzduchu, znížené vedomie a rozptýlenébublanie vysoko progresívneho pľúcneho edému(Obr.4). Cyanóza heliotropnej cyanózy nájdená vniektorí pacienti pred smrťou po heliotropnom fowerovisýto modrej alebo fialovej farby. Lekári si to tiež všimlipery a uši sú pred zaostrením intenzívne modrézvyšok tváre [31]. V liste kolegovi lekárovi, niektorí opísali farbu ako purpurovo-čiernu a jednuPoznamenal to škótsky lekár, ktorý pracuje v tábore Deven"Nie je ľahké rozlíšiť mužov od bielej farby." Inabnormálny pigment, lekár zistil, že cyanózaje v dôsledku rozsiahlych exsudácií v alveolách zabraňujúcichsprávne okysličenie pri opakovanej spektrografickej kontrolekrvi pacienta sa nenašla [60]. Dvaja psychiatrickístavov súvisiacich s akútnymi respiračnými poruchami.Syndróm rýchlej úmrtnosti (ARDS) a smrteľné prípady boliidentifikovaná bronchopneumónia. Sekundárna baktériainfekcia vedúca k bronchopneumónii spôsobilaväčšina úmrtí so zápalom pľúc, s výnimkou tých, ktorí zomreliv roku 1918 po epidémii H1N1 [60]. Počiatočná leukopo penii nasledovala bronchopneumónia leukocytóza [63]. Brundage a Shanks [64], zaznamenali mediánobdobie 7–10 nocí od začiatku ochorenia a niekoľko deaths>15 dní po nástupe, v spojení ssekundárny bakteriálny zápal pľúc, pre najviac postihnutýchpopulácia.
V prípade SARS, horúčka, zimnica, stuhnutosť, myalgia, suchosťtoxíny, dýchavičnosť, malátnosť a bolesť hlavy sú hlavnými rozlišovacími znakmiklinické znaky SRAS [65]. Populárnejšiesú bolesti hrdla, hnačka, rinorea, nevoľnosť, vracanie,a opuch [65]. U 40–70 percent pacientov so SARS vodnatábola prítomná hnačka. Stávalo sa to asi 7 dnípo nástupe choroby [18]. Dvaja pacienti vyhovujús epileptickým stavom boli zistené v sére acerebrospinálnej tekutiny. Starší pacienti infikovaní SARS-CoVmôže vyvinúť nízku chuť do jedla, zníženie celkovej pohody, pád zlomeniny a neistoty, ale nemusí byť schopnýzvýšiť horúčkovité reakcie u niektorých starších ľudí [66]. Na porovnanie, infekcia SARS-CoV bola zvyčajne miernau detí mladších ako 12 rokov. Naproti tomu infekcia u dospelýchdeti boli blízko tomu u dospelých [67]. SARS-CoV-acPožadovaná infekcia bola spojená s úmrtnosťou 25 percent.počas tehotenstva vysoký výskyt spontánnych potratov, predčasný pôrod a oneskorený vývojvnútromaternicové dieťa bez perinatálnej infekcie SARS-CoV[18].
Dospelí, ktorí sa nakazia MERS-CoV, môžuvyvinúť celý rad ochorení a závažnosti ochorenia, odasymptomatické až ľahké, stredné alebo ťažké (obr.4) [68]. Doba inkubácie je od 2 do 14 dní. Nízky stupeňhorúčka, nádcha, bolesť hrdla, suchý kašeľ a myalgiasa môže vyskytnúť u pacientov s miernymi infekciami. Pacienti szávažné infekcie majú syndróm akútnej pneumóniebolesť dýchania, multilaterálna schéma zlyhania orgánov achoroba. Okrem toho kolegovia členovia merajú zápal pľúcnia progresie hodnotením počtu röntgenových snímok pľúczóny u pacientov so závažnou infekciou, prejavujúce sa náhleprogresia po približne siedmich dňoch a závažnosťzápal pľúc. Symptómy vyvrcholili potom asi poštrnásť dní. MERS-CoV je vyšší v dolných dýchacích cestáchvzoriek ako v horných dýchacích cestáchvzorky. Bežné sú aj mimopľúcne charakteristikyvrátane myalgie. Späť k polovici všetkých MERS-CoVpacientov, tretinu kriticky chorých ľudí vrátane brušnýchbolesť, nevoľnosť, vracanie a hnačkaakútne poškodenie obličiek. Tretina sú gastrointestinálne aMERS-CoV v stolici možno nájsť [68].
Pokiaľ ide o COVID{0}}, únava a kašeľ sú myalgiaalebo únava [69], najčastejšie hlásené príznaky.Expektorácia, bolesť hlavy, hemoptýza a hnačkamenej časté príznaky [70, 71] a vo viac ako poloviciu pacientov sa vyvinula dýchavičnosť (obr.4). Výsledkykrvné testy ukázali, že bielych krviniek a lymfopéniaboli normálne alebo znížené [72]. Typická JIS admisCT snímky hrudníka boli bilaterálne, mnohopočetné lobulárne aoblasti konsolidácie podsegmentu [73]. Pacienti bez JISpreukázala obojstrannú zábrusovú nepriehľadnosť a subsegmentovúoblasti konsolidácie reprezentatívnym CT hrudníkazávery [74]. Laboratórne štúdie zistili, že najviacčastými príznakmi sú kašeľ (67,7 percenta) a horúčka (87,9 percenta)kým hnačka nie je častá.. 82,1 percenta JIS-prijatýchpacienti hlásili lymfopéniu [75].
Epidemiológia
Presný stupeň pandemickej chorobnosti a úmrtnosti na1918 nie je známy, pretože chrípka sa nelíši odiné ochorenia dýchacích ciest bez laboratórneho potvrdenia [76]. Analyzované vzorky z pitvy sú väčšinou z pľúctkaniva obetí, ktoré zomreli na jeseň r1918 [77]. Chýbajú aj epidemiologické detaily.Te fu nebolo ochorenie podliehajúce hláseniu ani sledované ochoreniepred pandémiou v akejkoľvek provinčnej alebo federálnej verejnostizdravotnícka organizácia. Po pandémii sa stala smrťouzjavné na jeseň 1918, Okrem toho spoločenstvázačali mať fyzické sily na registráciu prípadovchrípka [78]. Napriek tomu sa mnohé prípady vyhli spoľahlivému hláseniua/alebo včasné podávanie správ. V americkej verejnostiHealth Journal z januára 1919, napísal redaktor vv niekoľkých prípadoch boli údaje neúplné a klamlivépretože „požiadavka na intervenciu bola taká silná, želen veľmi málo z nich bolo ochotných zamerať sa v budúcnosti na výskum[60]. Hlásené od polovice osemnásteho storočia,významné pandémie sa vyskytli medzi 10. a40 rokov. Z nich pandémia „španielskeho fu“ v roku 1918bol najhorší na svete, zabil 20 až 40 miliónov alebo viacľudia (obr.5) [79].
V roku 2002 vypukla epidémia SARS s pôvodom v GuangdonguČína spustila hlavnú infekčnú chorobu číslo jeden21. storočia, s 916 úmrtiami medzi viac8098 pacientov v 29 krajinách. O desať rokov neskôr, 2254 laboratórne hlásenýchboli vyhlásené prípady MERS-CoVWHO s 800 úmrtiami v 27 krajinách od roku 2012 do 16september 2018 [80] (obr.5). Príznačne, vyše osemdesiatpercent nedávnych štúdií v oblasti virológie a genetikyinfekcie preukázali, že MERS-CoV ajNetopiere SARS by mohli byť potenciálnymi prírodnými rezervoármi. z potvrdenýchprípadov SARS, 22 percent boli zdravotníci vČína a viac ako 40 percent boli zdravotníciKanada [81]. Podobne nozokomiálny prenos MERSbol na Blízkom východe a v Kórei. Hlásené prípadyna Blízkom východe a v severnej Afrike prispeli všetcina ohniská v iných krajinách a ich prenosz dôvodu medzinárodného cestovania. SARS aj MERSprispeli k masívnemu verejnému zdraviu a hospodárstvu
ohniská [80].
Hostiteľské faktory súvisiace s morbiditou pandémiea kolísanie úmrtnosti
Imunitné reakcie a imunopatológia
Dendritické bunky (DC) významne prispievajú k vrodenýmimunitu a môže iniciovať veľké množstvo chemokínova cytokíny [82]. Tieto bunky sa môžu presunúť do lymfoidného tkanivatkaniva z periférneho tkaniva na aktiváciu populácie T-buniek [83]. Na druhej strane kľúč kimunitou proti vírusovým infekciám sú adaptívne T bunky[84]; CD4plusT bunky uľahčujú tvorbu vírusovo špecifickej protilátkyprodukcia T-dependentnou aktiváciou B buniek [85]. "CD8plusT bunky“ sú však cytotoxické, zabíjajúce vírusy[86].
Vrodené imunitné reakcie v čase chrípky môžubyť definovaný ako interakcia medzi sekrétmi sliznicea virióny, infekcie epitelových buniek a aktiváciainých typov obyvateľov epitelu alebo subepiteliálne vrstvy [87]. ktoré zahŕňajú lymfoidné „vrodené“ bunky,rezidentné makrofágy a dendritické bunky (vrátanealveolárne makrofágy) [87]. Po naverbovaní krvina miesta infekcie, iné bunkové typológie ako poly-morfonukleárne leukocyty a monocyty pôsobia [88]. Každý typ bunky zobrazuje inú množinu ponúksenzibilizovať prítomnosť vírusu a umožniť špeciálnu ochranufunkcie.
Okrem toho sú receptory strategicky umiestnenéniekoľko subcelulárnych komponentov, ako sú bunkové membrány,endozómy, cytozol a mitochondrie [89]. Toto povoľujehostiteľ namontovať obranu prispôsobenú inváziipatogén a vziať si jeho tropizmus, intracelulárny životný štýl,a reprodukčná stratégia zohľadňuje [90]. Pre fua iné infekcie, preto môžu vrodené reakciebyť pohodlne rozdelené do modulov, z ktorých každýzahŕňa špecifické typy buniek, receptory, molekulydefektory a vnútrobunkové kompartmenty. Thekomponenty chrípkového modulu prikladajú (1) solvable extracelulárne proteíny obsahujúce telesné tekutiny; (2)interferónový systém; (3) rôzne druhy cytokínova chemokíny schopné organizovať vrodenú odpoveď;(4) fagocytóza makrofágov a neutrofilov; (5) dendriticképrezentácia bunkového antigénu [91].
V prípade infekcie SARS, Ako vrodená azískané imunitné reakcie pomáhajú kontrolovať vírusya mierne ochorenia, dysregulácia cytokínov, vírusové cytopatické symptómy, downregulácia pľúc ACE 2, nepravidelnáimunitnú odpoveď a autoimunitné procesyviesť k vážnejšej chorobe a prípadnej smrti,progresia SARS môže byť spojená s bunkami sprostredkovanýmiimunita z T-pomocníka (T1) a zápalovéhyper vrodená odpoveď [92].
Výrazné zlepšenie "T1 a zápalucytokíny (interferón-g [IFN-g], interleukín-1 [IL-1],IL-6 a IL-12), spolu s výrazným nárastomchemokíny ako T1 chemokín, IFN-g, IL-10 indukovateľné,(IP-10) neutrofilný chemokín a monocytový proteín-1chemokínové príťažlivosti boli pozorované počas dvoch týždňovpo nástupe ochorenia v uskutočnenej výskumnej štúdiiu 20 dospelých infikovaných SARS-CoV [18].
Mechanizmy imunitnej odpovede spôsobené MERSStratégie infekcie CoV a imunitného únikuešte nie je úplne preskúmaný. Zvlášť zaujímavé,MERS-CoV vyvinul stratégie kontroly vrodenej imunitya zabraňovali alebo blokovali dráhy produkcie IFN [93]. Táto zručnosť môže byť v podstate zodpovednánajmä vysoká miera úmrtnosti pacientov s MERS-CoVtí s oslabenou imunitou. Raz ten vírusbol rozpoznaný ako Toll-like Receptors (TLR), jedenz dvoch rôznych adaptorových molekúlMyD88 (Myeloid Difference Primary Response 88) prípToll / Interleukín{0}} receptor (TIR-) obsahujúci doménuInterferón indukujúci adaptér- (TRIF). Molekulytiež aktivujú dráhy MAPK a NF-ŚB, ktoré podporujúvývoj prozápalových retardérova IFN“[93].
Počas infekcie COVID{0}} vrodenou aj adaptívnouimunitné bunky sú synergicky zapojené do antivírusovej ochranyodpoveď. Rýchlosť lymfocytov a podskupín Tbunky, ktoré zohrávajú významnú úlohu pri regulácii imunityodpoveď sa líši s potenciálnymi vírusovými patologickými mechanizmamiv závislosti od typu vírusu. Značný vzostupv neutrofiloch, leukocytoch a neutrofiloch-lymfocytochpomer (NLR) bol pozorovaný v závažných prípadoch COVID-19v porovnaní s miernymi prípadmi [96]. Výrazná lymfopénia,čo naznačuje poruchu imunitného systému,sa vyskytuje u väčšiny pacientov s COVID-19, najmä uťažké [97]. Preto sa zdá, že leukocytya neutrofily môžu posilniť cytokínovú búrku (CS)iné ako COVID-19 lymfocyty.Minulá práca znížila celkový počet lymfocytova T bunky u pacientov s infekciou SARS-CoV [94]. Nákaza SARS-CoV-2 môže mať za následokporuchy imunity dysregulácia ovplyvnením T bunkypodmnožiny [95–97]. Pozoruje sa významné zmiernenie T buniekpri COVID-19 a je výraznejšia v závažných prípadoch.U pacientov s COVID{0}} sú hladiny buniek (CD3plus, CD8plus), cytotoxické supresorové a pomocné T bunky (CD4plus, CD3plus), a regulačné T bunky sú nižšie ako normálne hladiny. Innaopak, pomocné T bunky a regulačné T bunky sú pozoruhodnénižšia u ťažkých pacientov ako u nezávažných pacientovako je znázornené na obr.6 [98]. Je známe, že regulačné T bunky súzodpovedný za udržiavanie imunitnej homeostázy potlačenímaktivácia, proliferácia a prozaklínadlofunkcia väčšiny lymfocytov, vrátane NK buniek, Tbunky CDplus4, T bunky CDplus8 a B bunky (obr.6) [99]. tiežpercento naivných pomocných T buniek sa zosilňuje.
Naproti tomu percento pamäťových pomocných T bunieka CD28pluscytotoxických supresorových T buniek klesá vzávažné COVID-19 bunky [100]. Rovnováha medzinaivné T bunky a pamäťové T bunky sú základomefektívnu imunitnú odpoveď. Okrem T buniek, zníženieNK buniek a B buniek sa pozoruje pri COVID-19 [101]. Celkovo tieto výsledky naznačujú, že SARS-CoV-2 indiUvedomte si, že SARS-CoV-2 je zodpovedný za imunitnú poruchuregulácia s indukciou aberantného cytokínu achemokínové odpovede [102] a zmeny lymfatických uzlínpodskupina cytokínov, z ktorých všetky by mohli viesť k búrkam cytokínova ďalšie poškodenie tkaniva [103]. Nadmerné zápalovéodpoveď s charakteristikou cytokínových búrok spôsobujezávažné ochorenie a zhoršuje prognózu COVID-19[104].
Vek
Hlavnú úlohu pri identifikácii zohráva vek postihnutého jedincariziko ich úmrtia počas chrípky v roku 1918pandemický. Vo všeobecnosti, keď sezónna chrípka smrťmiery sú vynesené ako funkcia veku populácie,získa sa krivka tvaru "U" s najvyššou úrovňouúmrtnosť pozorovaná medzi mladými a staršími [6]. Naopak, pandemické epidémie (v rôznej miere) súcharakterizované posunom letality smerom k mladšiemu vekuskupiny. To sa prejavilo najmä v roku 1918pandémiu, keď ju vo všeobecnosti mali mladí dospelí (15 – 30 rokov).vysoká miera úmrtnosti, že sa vytvorila krivka úmrtnosti "W". [6]. V prípade SARS boli infikovaní jednotlivci všetkých vekových skupín amedián veku bol menej ako štyridsaťpäť rokov. Zdravotná starostlivosťpracovníci predstavovali 22 percent všetkých prípadov v Hongkongu a22,8 percenta v Guangdongu. V Kanade a Singapure je to percentopostihnutých zdravotníckych pracovníkov bol vyšší, a to 43 percenta 41 percent, v uvedenom poradí. Rozdelenie podľa veku a pohlaviaSARS v Hong Kongu je nasledovný: 61,7 percenta pacientovdo 45 rokov, 21,2 percenta je vo veku 45 až 64 rokova zvyšok je starší ako 64 rokov. Jedenásť(8,14 percenta) zo 135 skorých komunitných prípadov bez jehotory kontaktu s pacientmi so SARS boli zoonotického typu.Miera úmrtnosti v Hongkongu stúpa s vekom ako v inýchsvetové regióny: 14,7 percenta medzi ľuďmi do 44 rokov, 21,4 percentamedzi 45 a 64 a 63,9 percenta nad 64 rokov. Skúsenosti zHongkong a ďalšie oblasti naznačujú, že úmrtia súspojené s koexistujúcimi ochoreniami v najstaršej vekovej skupine(>64 rokov) [105].
Požiadajte o viac:
E-mail:wallence.suen@wecistanche.com
Whatsapp/Tel: plus 86 15292862950

