Prognostická hodnota pentraxínu-3 u pacientov s COVID{1}}: Systematický prehľad a metaanalýza výskytu úmrtnosti
Nov 03, 2023
Abstrakt:Počas posledných troch rokov čelí ľudstvo jednej z najvážnejších zdravotných núdzových situácií v dôsledku globálneho šírenia koronavírusovej choroby (COVID-19). V tomto scenári predstavuje primárny cieľ výskum spoľahlivých biomarkerov úmrtnosti na COVID-19. Pentraxín 3 (PTX3), vysoko konzervovaný proteín vrodenej imunity, sa zdá byť spojený s horším výsledkom ochorenia. Na základe vyššie uvedeného tento systematický prehľad a metaanalýza vyhodnotili prognostický potenciál PTX3 pri ochorení COVID{6}}. Zahrnuli sme 12 klinických štúdií hodnotiacich PTX3 u pacientov s COVID{9}}. Z nášho výskumu sme zistili zvýšené hladiny PTX3 v porovnaní so zdravými jedincami, a najmä PTX3 bol ešte viac rozšírený v závažných prípadoch COVID{12}} než v nezávažných prípadoch. Okrem toho sme vykonali metaanalýzu, aby sme zistili, či existujú rozdiely medzi pacientmi na JIS a pacientmi, ktorí nie sú na COVID{16}} v úmrtiach súvisiacich s PTX{17}}. Skombinovali sme 5 štúdií s celkovým počtom 543 pacientov na JIS oproti 515 pacientom bez JIS. Zistili sme vysoko významné úmrtie súvisiace s PTX3-u osôb hospitalizovaných na JIS COVID-19 (184 z 543) v porovnaní s osobami bez JIS (37 z 515), s celkovým účinkom ALEBO: 11,30 [2. 00, 63,73];p = 0.006. Na záver sme sondovali PTX3 ako spoľahlivý marker zlých výsledkov po infekcii COVID-19, ako aj prediktor stratifikácie hospitalizovaných pacientov.

cistanche výhody pre mužov - posilnenie imunitného systému
Kľúčové slovods: Pentraxín{0}} (PTX3); COVID-19; SARS-CoV-2; úmrtnosť; imunopatológia
1. Úvod
SARS-CoV-2 vírus patrí do čeľade Coronaviridae, podčeľade Orthocoronavirinae a štrukturálne môže byť definovaný ako obalený pozitívny jednovláknový RNA vírus [1–3]. Počas posledných troch rokov viedlo šírenie SARS-CoV-2 k jednej z najzávažnejších núdzových situácií v oblasti verejného zdravia na svete, známej ako pandémia koronavírusovej choroby (COVID-19). Infekčná choroba COVID{9}}, prvýkrát hlásená v meste Wuhan (Čína) v decembri 2019, sa rýchlo rozšírila do zvyšku sveta a Svetová zdravotnícka organizácia (WHO) vyhlásila pandémiu COVID{11}} dňa 11. marca 2020 [4]. Najčastejšie klinické prejavy po inkubačnej dobe 2 až 14 dní (medián 5 dní) sú heterogénne a môžu sa výrazne líšiť v závažnosti medzi pacientmi, od úplne asymptomatického ochorenia až po prípady spojené s miernymi alebo stredne závažnými príznakmi podobnými chrípke, ako napr. kašeľ, horúčka, myalgia, bolesť hlavy, dyspnoe, bolesť hrdla, hnačka, nevoľnosť, vracanie, strata chuti a čuchu. Letalita sa odhaduje na priemerne 5 %, ale riziko závažnej/kritickej infekcie a úmrtia sa zvyšuje s vekom a v prítomnosti sprievodných ochorení, ako sú kardiovaskulárne ochorenia, cukrovka, hypertenzia, chronické respiračné ochorenie, rakovina atď. [5]. Okrem toho mnohé genetické a negenetické stavy u každého jednotlivca môžu ovplyvniť výsledok, čím sú ľudia vystavení vysokému riziku vzniku určitej závažnosti počas infekcie.

cistanche rastlina zvyšujúca imunitný systém
Niektoré z hlavných klinických problémov súvisiacich s COVID-19 boli doteraz čiastočne zmiernené zdokonalením dostupných farmakologických látok. Najmä rýchly vývoj vakcín a rýchla profylaxia veľkej časti populácie je v tomto smere takmer bezprecedentným úspechom modernej medicíny. Literárne údaje o účinnosti vakcín (51 štúdií zo 14 krajín) zdôraznili, ako očkovanie proti COVID-19 poskytlo významný, silný a predĺžený ochranný účinok pri hospitalizácii a hospitalizácii na jednotkách intenzívnej starostlivosti (JIS) a smrť na COVID-19 [6]. Napriek všetkým týmto úspechom pandémia COVID-19 stále predstavuje niekoľko významných výziev. Najrelevantnejšie obavy súvisiace s kontinuálnym pretrvávaním pandémie predstavujú prepuknutie nových vírusových variantov s vyššou infekčnosťou alebo mortalitou alebo menšou citlivosťou na v súčasnosti dostupné terapeutické látky [7]. Stále je potrebné vynaložiť úsilie na lepšie pochopenie patofyziologických mechanizmov COVID-19, ako aj imunitnej odpovede proti neustále sa meniacemu vírusu, na identifikáciu nových farmakologických nástrojov a na nájdenie spoľahlivých prognostických prediktorov ochorenia a/alebo výskyt dlhodobých zmien. Pentraxín-3 (PTX3), základná zložka humorálnej vrodenej imunity, bol uznaný v rezistencii voči vybraným patogénom a regulácii zápalu [8,9]. PTX3 patrí do superrodiny pentraxínov, čo je evolučne konzervovaná skupina proteínov so základnými úlohami pri rozpoznávaní vlastných a iných antigénov. Podobnosť s krátkym pentraxín C-reaktívnym proteínom (CRP) podnietila skúmanie užitočnosti PTX3 ako markera pri rôznych ľudských stavoch infekčného alebo zápalového pôvodu. Na rozdiel od CRP, produkovaného v podstate pečeňou ako odpoveď na interleukín (IL)-6 počas reakcie akútnej fázy [10], PTX3 je rýchlo produkovaný niekoľkými typmi buniek vrátane myeloidných buniek, endotelových buniek a respiračného epitelu buniek, najmä v reakcii na IL-1, tumor nekrotizujúci faktor, mikrobiálne molekuly a poškodenie tkaniva [8,9]. Lokálna produkcia rôznymi typmi buniek v zápalových miestach a uvoľňovanie vopred vytvoreného proteínu neutrofilmi v reakcii na primárne prozápalové cytokíny alebo mikrobiálne rozpoznanie vysvetľujú rýchlosť zvýšenia PTX3 pri týchto stavoch. Spomedzi svojich úloh v organizme sa PTX3 podieľa na rozpoznávaní a eliminácii patogénov, pôsobí ako opsonín, a teda stimuluje fagocytózu [11]. PTX3 významne zosilňuje odpoveď neutrofilov [12], čím prispieva k zosilneniu a predĺženiu zápalovej odpovede. Táto aktivita striktne závisí od aktivácie alternatívnej komplementovej dráhy, hlavne prostredníctvom väzby na komplementový receptor 3 (CD11b/CD18) [12]. PTX3 môže interagovať so zložkou komplementu 1q (C1q) [13] na základe mechanizmu nezávislého od vápnika, čím indukuje aktiváciu klasickej dráhy komplementu. Zatiaľ čo PTX3 môže prispievať k odstraňovaniu patogénov, môže tiež zhoršiť závažnosť patologických zápalových reakcií [14]. Aberantná odpoveď organizmu na infekciu môže viesť k stavu, akým je syndróm systémovej zápalovej odpovede (SIRS), ktorý v závažných prípadoch môže viesť k sepse. Aby sa to potvrdilo, vysoké plazmatické koncentrácie PTX3 boli spojené so závažnosťou ochorenia a mortalitou pri rôznych patologických stavoch [15,16]. Ukázalo sa, že PTX3 pôsobí ako biomarker aktivity ochorenia pri zápalových stavoch zahŕňajúcich cievne riečisko, od aterosklerózy po vaskulitídu [16,17] a tiež pri zmenách imunity. Imunitný systém je rozhodujúci pri ochrane organizmu a účinnej odpovedi na vírusové respiračné infekcie a v tomto smere nie je výnimkou ani infekcia SARS-CoV{50}}. Imunitné bunky sú vybavené súborom špecifických extracelulárnych a cytosolických receptorov, tj Toll-like receptormi (TLR), RIG-like receptormi (RLR), NOD-like receptormi (NLR) a chýbajú pri melanóme 2 (AIM2) receptory (ALR), čo im umožňuje včas reagovať na nešpecifické zápalové signály, ako sú molekulárne vzory spojené s patogénmi (PAMP) a molekulárne vzory spojené s poškodením (DAMP). Po interakcii s týmito vírusovými stimulmi nastáva špecifická imunitná odpoveď s uvoľnením množstva rozpustných faktorov, cytokínov, chemokínov a komplementového systému [18]. Bolo poskytnutých niekoľko dôkazov, ktoré dokazujú, že imunologická pamäť SARS-CoV-2 môže trvať aj viac ako 6 mesiacov po infekcii [19,20]. Štúdie špecificky hodnotiace imunitnú pamäť na SARS-CoV-2 skutočne odhalili, že pamäťové CD4+ T bunky a pamäťové CD8+ T bunky bolo možné detegovať 6 mesiacov po infekcii u 90 % a 70 % pacientov v rekonvalescencii a pamäťových B buniek takmer u všetkých pacientov v rovnakom časovom rámci [19,20]. Okrem vyššie uvedenej imunologickej pamäte existujú dôkazy, že infekcia SARS-CoV{76}} môže vyvolať dlhotrvajúce abnormality imunitnej odpovede, ktoré zostávajú zistiteľné 11 mesiacov po infekcii [21], čo tiež spôsobuje jasný posun v CD{{80} } a CD{81}} buniek 3 mesiace po infekcii [22]. Tento klinický obraz, známy ako post-COVID{86}} syndróm, zahŕňa rôzne neurologické, kardiovaskulárne, autozápalové, renálne a endokrinné prejavy, ktoré môžu pretrvávať niekoľko mesiacov [23].
Vzhľadom na vzorec PTX3 sa zdá, že sa zvýšil počas ochorenia COVID-19 a takéto vysoké hladiny súviseli s vyšším rizikom úmrtnosti [24]. PTX3 by teda mohol byť možným prediktorom klinického priebehu pacientov po infekcii. Iné štúdie navrhujú PTX3 ako diskriminačný faktor stratifikácie nemocníc, čo naznačuje, ako by jeho vysoké hladiny súviseli s pravdepodobnejším prijatím na JIS ako na iné oddelenia. Špecifický vplyv PTX3 na progresiu COVID-19 je však stále nejasný z dôvodu nedostatku veľkých multicentrických štúdií, ako aj niekoľkých štúdií v literatúre z dôvodu krátkeho času od pandémie. Preto je stále potrebné definovať, či má PTX3 prognostickú hodnotu a evidentný klinický význam. Cieľom tohto systematického prehľadu bolo posúdiť hodnotu PTX3 ako diagnostického a prognostického faktora pri infekcii COVID-19 a tiež prostredníctvom kvantitatívnej metódy (metaanalýzy) diskutovať o súvisiacom zvýšení úmrtnosti u rôznych hospitalizovaných pacientov. Presné hodnotenia hladín PTX3 u pacientov s COVID{12}} môžu byť užitočné pri poskytovaní novej perspektívy pre klinickú prax a sledovanie.

cistanche výhody pre mužov - posilnenie imunitného systému
Kliknite sem pre zobrazenie produktov Cistanche Enhance Immunity
【Požiadať o viac】 E-mail:cindy.xue@wecistanche.com / Whats App: 0086 18599088692 / Wechat: 18599088692
2. Metódy
2.1. Metódy
Bibliografické databázy PubMed (MEDLINE) a Embase (OVID) boli skontrolované na účely vyhľadávania literatúry. Ako usmernenia na podávanie správ o výskumnej stratégii štúdií sme použili Preferované položky hlásenia pre systematické preskúmanie a protokoly metaanalýzy (PRISMA-P). APC a AA vykonali bibliografické vyhľadávanie na základe kritérií oprávnenosti zhrnutých v tabuľke 1 a brali do úvahy iba články napísané v angličtine.
Tabuľka 1. Opis kritérií oprávnenosti.

Dvaja experti na obsah (MC a EE) navrhli stratégiu vyhľadávania a dohliadali na štúdiu. Neboli uložené žiadne kritériá geografického vylúčenia ani dočasné obmedzenia. V PubMed (MEDLINE) a Embase (OVID) sa výrazy súvisiace s PTX3 a COVID-19 skúmali pomocou špecifických kľúčových slov uvedených v tabuľke 2.
Tabuľka 2. Kombinácie kľúčových slov použité počas stratégie vyhľadávania.

2.2. Výber štúdia
Po vyhľadávaní PubMed (MEDLINE) a Embase (OVID) sme odstránili duplikáty a potom dvaja autori recenzií (APC a AA) individuálne preverili názvy a abstrakty všetkých identifikovaných záznamov, aby odstránili články, ktoré neboli relevantné. Následne sme preskúmali články v plnom znení, aby sme vybrali záznamy, ktoré najviac zodpovedali kritériám oprávnenosti; protichodné názory boli vyriešené sprostredkovaním tretieho autora recenzie (EE). Extrakciu údajov zo zahrnutých článkov vykonali dvaja autori (APC a AA). Z 12 zahrnutých štúdií sme zhromaždili nasledujúce údaje: názov, autor(i), rok vydania, spádová oblasť štúdie (tj geografická zóna), študovaná populácia (tj rôzne populácie pacientov s COVID alebo zdravých jedincov, JIS vs. -JIS).
2.3. Posúdenie rizika zaujatosti
Kvalita vhodných záznamov opísaných v tomto systematickom prehľade bola individuálne hodnotená dvomi recenzentmi (APC a AA) pomocou stupnice Newcastle Ottawa (NOS; pozri doplnkovú tabuľku S1), ako už bolo opísané [25,26]. Na základe tohto úsudku bola hodnota štúdie klasifikovaná ako nízka, stredná alebo vysoká. Rozdiely v priraďovaní skóre boli vyriešené zapojením tretieho autora recenzie (EE). Po hodnoteniach autorov nebol žiadny z článkov považovaný za vysoko rizikový.
2.4. Metódy syntézy dát pre metaanalýzu
Na štatistickú analýzu v kvantitatívnej syntéze sme použili mieru šancí (OR) a model náhodných efektov s Mantel-Haenszelovou metódou. Nakoniec sme získali združené odhady variantného účinku (OR) so súvisiacim 95% intervalom spoľahlivosti (CI). Heterogenita bola odhadnutá prostredníctvom grafického skúmania lesných pozemkov a potom hodnotená pomocou štatistiky I2, ako bolo opísané vyššie [25,26]. Na vykonanie metaanalýzy získaných údajov bol použitý Review Manager (Rev Man. Version 5.4. Copenhagen: The Nordic Cochrane Centre, The Cochrane Collaboration, 2014).
3. Výsledky a diskusia
3.1. Zistenia zo systematického vyhľadávania
Celý proces skríningu sme ilustrovali na obrázku 1 prostredníctvom vývojového diagramu PRISMA-P. Počas prvého kroku vyhľadávania pomocou vyššie uvedených kľúčových slov sme identifikovali 2390 záznamov v databázach PubMed (MEDLINE) a Embase (OVID). Po odstránení duplikátov sme získali 1359 záznamov, ktoré boli analyzované podľa názvu a abstraktu, aby sa vyhodnotila ich vhodnosť. Po prečítaní názvu a abstraktu sme vylúčili 1326 článkov, pretože neboli relevantné pre našu recenznú otázku. Potom sme preskúmali oprávnenosť celého textu 33 článkov, pričom sme vylúčili 21 záznamov, pretože nezodpovedali stanoveným kritériám zaradenia a vylúčenia. Do nášho systematického prehľadu sme zahrnuli 12 štúdií, ako ukazuje vývojový diagram PRISMA uvedený na obrázku 1, odkedy sme hodnotili PTX3 u pacientov s COVID{11}} a konkrétne porovnávali pacientov s COVID{12}} so zdravými jedincami alebo analyzovali hladiny PTX3 v stratifikácii COVID{14}} hospitalizovaných. Vykonali sme aj metaanalýzu výskytu úmrtnosti súvisiacej s hladinami PTX3 u rôznych hospitalizovaných pacientov s COVID{17}}. Na tento účel sme z 12 štúdií zahrnutých do systematického prehľadu vybrali iba 5 záznamov, ktoré hodnotili hladiny PTX3 na JIS v porovnaní s pacientmi bez JIS.

Obrázok 1. Vývojový diagram PRISMA. Obrázok popisuje každý krok stratégie vyhľadávania a skríningu, celý proces prebiehal podľa smernice PRISMA-P
3.2. Hodnotenie zahrnutých štúdií v systematickom prehľade
V každej zahrnutej štúdii boli hladiny PTX3 hodnotené laboratórnym testovaním pri prijatí do nemocnice. Celkovo boli hodnoty PTX3 významne vyššie u pacientov s COVID-19 ako u zdravých jedincov, čo znamená zmenu imunozápalového procesu po infekcii, pri ktorej by PTX3 mohol pôsobiť ako hlavný faktor. Okrem toho sme pri analýze stratifikácie hospitalizovaných pacientov (v štúdiách, v ktorých bola prezentovaná) zaznamenali, že PTX3 sa značne zvýšil u pacientov na JIS vyžadujúcich mechanickú ventiláciu a primeranú starostlivosť vzhľadom na život ohrozujúci stav. Hladiny PTX3 boli mierne nižšie u pacientov prijatých na iné oddelenia. Hodnoty PTX3 sú zhrnuté v tabuľke 3, zatiaľ čo podrobný opis zahrnutých štúdií je uvedený v časti Diskusia.
Tabuľka 3. Tabuľka sumarizujúca články zahrnuté do systematického prehľadu a súvisiace hladiny PTX3 u rôznych subjektov.

Tabuľka 3. Pokr.

Tabuľka 3. Pokr.

3.3. Metaanalýza výskytu úmrtnosti medzi rôznymi populáciami COVID-19
Zo skríningu vykonaného na identifikáciu štúdií vhodných na metaanalýzu len päť záznamov vyhovovalo kritériám zaradenia (kvantitatívne hodnotenie PTX3 na JIS oproti hospitalizovaným pacientom bez JIS). V zahrnutých štúdiách bol PTX3 navrhnutý ako možný prognostický faktor u pacientov s COVID-19 a jeho hladiny sa zisťovali rutinnými laboratórnymi testami.
Týchto päť článkov objasnilo PTX3 ako prediktor stupňa hospitalizácie, a preto jeho vysoké hodnoty často súviseli s pacientmi vyžadujúcimi mechanickú ventiláciu a starostlivosť na JIS. Vzhľadom na tieto predpoklady sme chceli prostredníctvom kvantitatívnej analýzy preskúmať stupeň úmrtnosti medzi subjektmi COVID{1}} prijatými na JIS a porovnať ich s osobami bez JIS. Ako je znázornené na lesnom pozemku (obrázok 2), OR sa pohybujú medzi 2,40 – 236,47, a hoci heterogenita bola značná (I2=86 %), celkový OR bol 11,30 (95 % CI: 2).{13} }–63,73) a test celkového účinku bol p=0,006. Tento výsledok odhalil silnú štatistickú významnosť, ktorá naznačuje výrazne zvýšenú mieru úmrtnosti pacientov na JIS v porovnaní s pacientmi bez JIS, čím demonštruje, že vysoké hladiny PTX3 u pacientov s COVID{20}} prijatých na JIS okrem predpokladaného stupňa hospitalizácie sú tiež spoľahlivým prediktorom úmrtia pacientov.
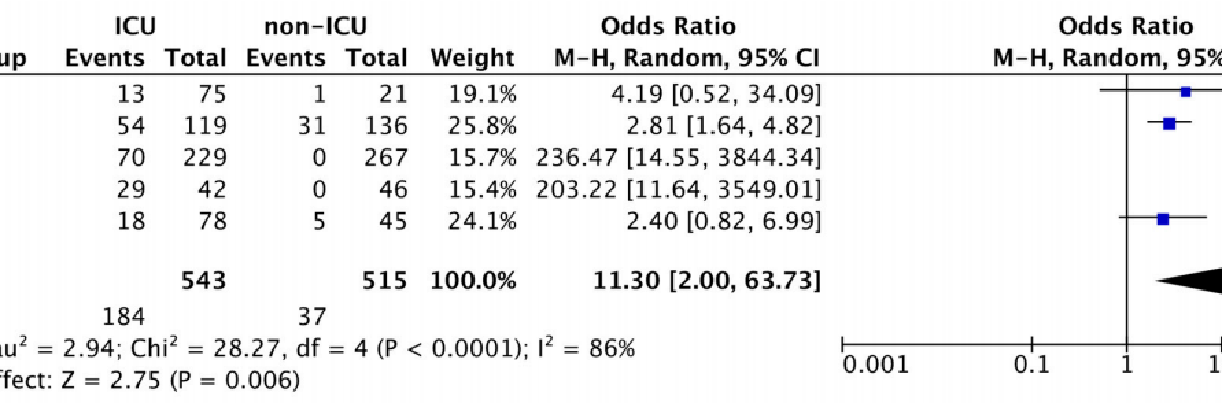
Obrázok 2. Lesný graf štúdií zahrnutých do kvantitatívnej syntézy. Lesný pozemok opisuje výskyt úmrtnosti medzi pacientmi na JIS a pacientmi bez JIS, u ktorých sa hodnotili hladiny PTX3. Smrť pacientov sa označuje ako udalosti v porovnaní s celkovým počtom subjektov. Štvorce zobrazujú odhad účinku (OR) s veľkosťou každého modrého štvorca zodpovedajúcou váhe pridelenej každej štúdii v metaanalýze. Horizontálne čiary predstavujú 95 % CI zodpovedajúce každému odhadu účinku. Čierny diamant predstavuje celkový efekt zásahu, pričom jeho šírka predstavuje celkový 95% CI. Štatistika I2 predstavuje mieru heterogenity. Celkový efekt ALEBO: 11,30 [2.{10}}, 63,73]; p=0.006.
PTX3 sa ukázal ako silný nezávislý prediktor smrti lepší ako konvenčné biomarkery, ako sú CRP a IL-6. V skutočnosti, vykonaním celkového hodnotenia piatich štúdií zahrnutých do metaanalýzy, len PTX3 možno navrhnúť ako presný prognostický faktor, čo vedie ku konzistentným a štatisticky významným výsledkom, na rozdiel od CRP a IL-6, ktoré boli variabilné a niekedy slabo spojené s úmrtnosťou. Tieto údaje si určite zaslúžia ďalšie klinické skúmanie.
3.4. Diskusia
SARS-CoV-2 je agent zodpovedný za pandemickú chorobu COVID-19. Vírus sa môže zamerať na dýchací systém a šíriť sa z človeka na človeka prostredníctvom respiračných kvapôčok od infikovaných jedincov [39]. Z niekoľkých lokalizovaných prípadov na konci roka 2019 sa choroba v prvých mesiacoch roku 2020 rýchlo rozšírila po celej planéte. Oficiálne údaje WHO k 13. januáru 2023 uvádzajú 661 545 258 potvrdených prípadov COVID{{11 }}, vrátane 6 700 519 úmrtí.
Jedným z primárnych mechanizmov závažných klinických komplikácií je aberantná zápalová odpoveď vyplývajúca z rýchlej replikácie vírusu v alveolárnych bunkách, ktorá spúšťa počiatočnú Th1 odpoveď a následnú masívnu infiltráciu makrofágov a neutrofilov pľúcnym tkanivom, ako aj sekréciu pro- zápalové cytokíny [40]. Tento patologický proces, známy ako „cytokínová búrka“, prispieva k závažným a život ohrozujúcim pľúcnym a mimopľúcnym komplikáciám, ktoré v konečnom dôsledku vedú k stavu multiorgánového zlyhania [41,42]. Navrhovaná patogénna hypotéza naznačuje, že dlhotrvajúci zápalový stav spojený s hypersekréciou cytokínov môže byť zodpovedný za stav stredného latentného zápalu, ktorý by zase mohol viesť k symptómom súvisiacim s chronickým zápalom [43]. Hodnotenie molekúl humorálnej vrodenej imunity, ako je PTX3, v kontexte ochorenia COVID-19, by mohlo byť užitočné pri monitorovaní prognózy.

cistanche výhody pre mužov - posilnenie imunitného systému
Cieľom tohto systematického prehľadu je preto analyzovať a zhrnúť prognostickú hodnotu PTX3 u pacientov s COVID-19 a tiež objasniť súvisiace klinické výsledky u rôznych pacientov hospitalizovaných na COVID-19. Hoci je šírenie COVID-19 obmedzené len na tri roky, našli sme niekoľko článkov, ktoré analyzovali úlohu proteínu PTX3 u postihnutých pacientov. Oprávnené pokroky naznačili potenciálny význam PTX3 ako spoľahlivého prognostického faktora u pacientov s COVID-19, ako aj u rôznych stupňov závažnosti ochorenia, ako je JIS, v porovnaní s pacientmi bez JIS. Brunetta a kol. hodnotili prítomnosť PTX3 u pacientov s COVID-19 [28]. Autori vykonali štúdiu na dvoch kohortách pacientov, z ktorých prvá pozostávala z 96 subjektov prijatých do Humanitas Clinical and Research Center (Milán, Taliansko), druhá nezávislá kohorta 54 jednotlivcov prijatých do ASST Papa Giovanni XXIII (Bergamo, Taliansko) . Zvyšujúce sa plazmatické koncentrácie PTX3 boli objavené u 96 pacientov s COVID{15}} (medián 17,3 ng/ml; p < 0,0001) spolu so značným zvýšením obsahu IL-6 (p {{ 21}},017), zatiaľ čo hodnotenie CRP neukázalo výrazné výsledky (p=0,082). Spomedzi rôznych analyzovaných zápalových markerov sa PTX3 skutočne ukázal ako silný nezávislý prediktor 28-dňovej mortality v multivariačnej analýze [28]. Hladiny PTX3 sa zdali vyššie u mŕtvych pacientov v porovnaní s prežívajúcimi jedincami (medián 39,8 ng/ml), ale aj u pacientov na JIS v porovnaní s pacientmi na oddelení [28]. Tieto údaje boli ďalej overené v kohorte 54 pacientov, PTX3 viedol k lepšiemu prediktoru mortality (p=0,026) ako CRP (p=0,203) a IL-6 ( p=0.099) [28]. Genc a kol. hodnotili predikčnú hodnotu PTX3 pri COVID-19 pneumónii [31]. Štúdia sa uskutočnila na 88 potvrdených pacientoch COVID{46}}, z ktorých sa neskôr zistilo, že 59 prežilo a 29 neprežilo [31]. Veľmi vysoké hladiny PTX3 sa našli u všetkých jedincov COVID{52}} s mediánom 3,66 ng/ml; okrem toho boli takéto hladiny významne vyššie u nepreživších v porovnaní s preživšími (p=0,045) [31]. Kukla a kolegovia odhadli niekoľko biochemických parametrov, vrátane PTX3, pomocou imunoenzymatických metód [34]. Na tento účel bolo do štúdie zaradených 70 potvrdených pacientov s COVID{62}} (43 žien a 27 mužov) a 20 zdravých dobrovoľníkov (10 žien a 10 mužov) [34]. V prvých analýzach medzi pacientmi s COVID-19 (2337,7 pg/ml) a pacientmi bez COVID{73}} (2030,9 pg/ml) boli identifikované mierne rozdiely v PTX3, hoci nie štatisticky významné (p {{77} }.55) [34]. Zatiaľ čo podľa predchádzajúcich výsledkov boli konzistentné koncentrácie PTX3 v sére zistené u 9 pacientov s COVID{82}}, ktorí potrebovali starostlivosť na JIS (4768,9 pg/ml) v porovnaní so 61 pacientmi, ktorí ju nepotrebovali (2278,2 pg/ml) [34] . Autori však neuviedli žiadny rozdiel v koncentrácii PTX3 medzi pacientmi s pneumóniou a zdravými jedincami. V kohorte na JIS analyzovanej Gutmannom a kol. sa PTX3, stanovený pomocou ELISA, ukázal ako proteín pozitívne spojený s úmrtnosťou na COVID{91}} [32]. Populáciu tvorilo 123 pacientov s COVID, z ktorých 78 bolo na jednotke intenzívnej starostlivosti a 45 na oddelení intenzívnej starostlivosti. Zo 78 na JIS prežilo 60 a 18 zomrelo po infekcii [32]. Kontrolnú skupinu tvorilo 55 pacientov bez COVID{103}}, z ktorých 25 bolo hospitalizovaných na jednotke intenzívnej starostlivosti, zatiaľ čo 30 bolo mimo JIS [32]. Ak vezmeme do úvahy analýzu nemocničného oddelenia na JIS, u nepreživších pacientov s COVID{109}} bol PTX3 značne zvýšený (4,93 ng/ml) v porovnaní s hladinami prežívajúcich pacientov, ktoré boli 2,16 ng/ml [32]. PTX3 posúva infekcie COVID{117}} k chronickejším a viac invalidizujúcim stavom. Jeho zvýšenie teda vedie k vyššiemu riziku vzniku COVID{118}} pneumónie (zápal pľúc: 2,92 ng/ml oproti žiadnej pneumónii: 2,28 ng/ml), ako aj vyššiemu riziku hospitalizácie na oddeleniach JIS (starostlivosť na JIS: 4,77 ng/ml oproti starostlivosti bez JIS: 2,30 ng/ml) [35]. Moulana a kolegovia našli zvýšené hladiny PTX3 v sére život ohrozujúcich pacientov s COVID{130}}. Z celkového počtu 98 jedincov zaradených do štúdie bolo 14 pacientov hospitalizovaných na JIS, 59 pacientov bolo hospitalizovaných na oddeleniach bez JIS a 25 jedincov predstavuje zdravú kontrolnú skupinu [37]. Z údajov získaných pomocou súpravy ELISA vykonanej na vzorkách séra mali pacienti na JIS vyššie hladiny PTX3 v porovnaní s pacientmi bez JIS (1957 ± 1769 pg/ml oproti 1220 ± 1784 pg/ml) alebo zdravými jedincami (1957 ± 1769 pg/ ml oproti 275 ± 167 pg/ml) [37]. V štúdii Assandriho a spol. sa zistil prekrývajúci sa trend, pacienti prijatí na JIS skutočne vykazovali vyššie koncentrácie PTX3 v porovnaní s pacientmi bez JIS (stredná hodnota 35.{151}} ng/ml oproti 10,61 ng/ml) [27]. Kontrolní jedinci vykazovali medián 2,30 ng/ml [27]. Okrem toho autori zdôraznili vyššiu presnosť PTX3 v porovnaní s CRP, laktátdehydrogenázou (LD) a feritínom pri identifikácii pacientov na JIS. Okrem toho z výsledkov laboratórnych testov zaradených pacientov sa PTX3 ukázal ako jeden z najspoľahlivejších, na rozdiel od iných bežne používaných zápalových markerov, ako je IL-6 (p=0.551). Nepriaznivý výsledok na všeobecnom oddelení a na JIS bol teda spojený so zmenami v koncentráciách PTX3, ako sa prehĺbilo v prospektívnej kohortovej štúdii de Bruin et al. [29]. PTX3 bol spoľahlivým biomarkerom pri predpovedaní nepriaznivých výsledkov na všeobecnom oddelení a tiež v súvislosti s úmrtím na JIS [29]. Na druhej strane sa nezistili žiadne významné rozdiely v hladinách CRP medzi preživšími a nepreživšími v kohorte na JIS (p=0.24), čo poukazuje na vysokú variabilitu tohto biomarkera pri predpovedaní úmrtnosti na COVID{170} } problémov.
Táto štúdia teda prispieva k charakterizácii klinického priebehu pacientov so závažným COVID súvisiacim s PTX{{{{2{25}}}}}-19. V tomto zložitom klinickom obraze vstupuje do hry niekoľko dráh vrátane chemotaxie a produkcie interleukínu, ale aj endoteliálnej dysfunkcie, komplementového systému a imunotrombózy. Všetky tieto faktory, ak nie sú udržiavané pod kontrolou prostredníctvom primeranej profylaxie, robia z COVID-19 veľmi nepredvídateľné ochorenie, ktoré je založené na interindividuálnej náchylnosti od asymptomatickej až po respiračné zlyhanie alebo smrť. Meranie PTX3 do 4 dní od prijatia sa ukázalo ako prediktívna hodnota mechanickej ventilácie a 30-dňovej mortality v porovnaní s klinickými parametrami a inými markermi zápalu [33]. Ako uviedli Hansen a kolegovia, u pacientov so smrťou bola stredná koncentrácia PTX3 pri prijatí 19,5 ng/ml (IQR: 12,5–33,3) oproti 6,6 ng/ml (IQR 2,9–12,3) (p < 0).{38 }}001) pre tých, ktorí prežili [33], ako aj hladiny IL-6 viedli k zvýšeniu u tých, ktorí neprežili v porovnaní s tými, ktorí prežili (p < 0).{{93 }}001). V opačnom prípade sa nezistila žiadna významná zmena hodnôt CRP (p=0.18). Najnovšie pokroky, okrem potvrdenia predchádzajúcich poznatkov, zdôraznili zapojenie PTX3 do aktivácie a regulácie komplementového systému a zároveň zopakovali jeho dôležitú úlohu v patogenéze COVID-19. Plazmatické hladiny PTX3 boli významne spojené so závažnosťou a mortalitou COVID{32}} (p < 0,05) [30]. Závažná skupina mala vyššie hladiny PTX3 (medián: 987,0 pg/ml) v porovnaní so stredne ťažkou skupinou (medián: 570,5 pg/ml) (p=0,0004) [30]. Hladiny PTX3 pri prijatí boli pozorované ako 3,3-krát vyššie u pacientov, ktorí zomreli ako u tých, ktorí prežili (2233 pg/ml [n=25] oproti 663,2 pg/ml [n=144], p < 0,0001 ) [30]. Okrem toho Feitosa a kol. naznačili, že hladiny PTX3 významne korelovali s IL-6, IL-8, IL-10, CRP, celkovým počtom leukocytov, pomerom neutrofilov k lymfocytom, močovinou, kreatinínom, feritínom, dĺžkou hospitalizácie pobyt a vyššia dychová frekvencia (p < 0,05) [30]. PTX3 bol spojený s rizikom úmrtia pacientov (na 10 ng/ml, HR 1,08; 95 % CI 1,04–1,11; p < 0,001) a v pomere smrť/mechanická ventilácia (HR 1,04; 95 % CI 1,01–1,07; p=0 0,011), nezávisle od iných prediktorov nemocničnej mortality, vrátane veku, Charlsonovho indexu komorbidity, D-diméru a CRP podľa hodnotenia Lapaduly a kolektívu [36]. Pacienti s hladinami PTX3 nad optimálnou hraničnou hodnotou 39,32 ng/ml mali signifikantne vyššiu mortalitu ako ostatní (55 % vs. 8 %, p < 0,001) [36]. V multivariačnej analýze smrti bol PTX3 skutočne najvýznamnejším faktorom v porovnaní s CRP alebo D-dimérom [36]. Okrem toho boli vyššie plazmatické hladiny PTX3 zistené u 14 pacientov s následnými trombotickými komplikáciami [36]. Sulicka-Grodzicka et al., spôsobom v súlade s predchádzajúcou prácou, našli vyššie hladiny PTX3 u pacientov s ťažkým COVID{104}} ako u pacientov s nezávažným COVID{106}} [38]. Autori hodnotili sekvenciu zápalových reakcií pri akútnom COVID{108}} prostredníctvom 28-dňového sledovania, pričom zistili, že vymiznutie zápalu v skupine stredne závažnej/závažnej infekcie SARS-CoV2 bolo spojené so znížením PTX3 sérové koncentrácie [38]. Autori vykonali analýzu časového priebehu PTX3 1., 7. a 28. deň po infekcii [38]. Ich výsledky odhalili konštantný a progresívny pokles PTX3 od 1. dňa do 28. dňa [38]. Na druhej strane, pri analýze zápalových markerov medzi nezávažným COVID{125}} a ťažkým COVID{126}} bol PTX3 významný iba v 1. deň, na rozdiel od TNF a IL-1, ktoré sa tiež zvýšili 28 dní po infekcii [38]. Podobným spôsobom Hansen a kol. hlásili hladiny PTX3 v priebehu času pre pacientov, ktorí prežili COVID{134}} a ktorí neprežili, počas 14 dní po prijatí do nemocnice, s mierne odlišnou kinetikou [33]. Vzhľadom na to, že väčšina zahrnutých štúdií nevykonáva 28-dňovú následnú analýzu, domnievame sa, že na stanovenie dlhodobého kurzu PTX3 sú potrebné budúce štúdie, aby sa poskytli konzistentnejšie závery. Hladiny PTX{142}} sa zvyčajne zvyšujú po 6–8 hodinách zápalového procesu a môžu viesť k uvoľneniu určitých cytokínov, ktoré môžu spôsobiť dlhotrvajúcu búrku cytokínov [31]. V opačnom prípade je potrebné počkať viac ako jeden a pol dňa na zvýšenie iných biomarkerov, ako je CRP na spustenie zápalu [31]. Z týchto vyhlásení sa zdá byť jasná skorá upregulácia PTX3 medzi inými zápalovými markermi, teda predpokladá sa, ako by jej zníženie mohlo súvisieť s riešením COVID{148}}. Ak komplexne preskúmame naše zistenia, PTX3 sa javí ako najkonzistentnejší biomarker pri určovaní výsledku ochorenia v porovnaní s inými známymi biomarkermi, ako sú CRP alebo IL{150}}. Na rozdiel od PTX3 hodnotenie CRP alebo IL{152}} medzi rôznymi kohortami pacientov s COVID{153}} neviedlo vždy k štatisticky významným výsledkom, čo odhaľuje vysokú heterogenitu výsledkov týkajúcich sa týchto dvoch biomarkerov.

cistanche tubulosa - zlepšenie imunitného systému
Výsledkom kombinácie 5 štúdií v metaanalýze bolo celkovo 543 pacientov na JIS oproti 515 pacientom bez JIS. Uskutočnená metaanalýza ukazuje, že existuje významný nárast úmrtnosti u pacientov na JIS (184 z 543) v porovnaní s pacientmi bez JIS (37 z 515); ALEBO: 11,30 (95 % CI: 2.00–63,73; p=0,006). Tento aspekt, ako uvádzajú zahrnuté štúdie, priamo koreluje so zvýšením sérového PTX3, ktorý preto okrem toho, že je užitočný pri predpovedaní nemocničnej stratifikácie pacienta, predstavuje aj prediktor smrti. V tejto štúdii je však potrebné vyriešiť niektoré obmedzenia, po prvé niekoľko zahrnutých štúdií. Zozbierané zistenia môžu byť vystavené potenciálnemu skresleniu v dôsledku rôznych premenných. Zahrnuli sme štúdie založené na pacientoch kohorty COVID{21}}, ktoré sa môžu líšiť, pokiaľ ide o vek, pohlavie, etnickú príslušnosť, vírusové varianty a iné klinické komplikácie, ako aj individuálnu farmakologickú liečbu. Napríklad medzi zahrnutými záznamami bol čas odberu vzoriek heterogénny a na detekciu hladín PTX3 sa mohli použiť experimentálne postupy s rôznou citlivosťou. Žiadna zo zahrnutých štúdií skôr neprezentovala rodovo špecifickú stratifikáciu, takže pomocou tohto parametra sme nemohli vykonať analýzu podskupín. Okrem toho niektoré potenciálne biomarkery neboli analyzované, takže priame porovnanie s inými konvenčnými alebo nekonvenčnými biomarkermi nebolo zahrnuté do tejto štúdie. Napriek niekoľkým faktorom, ktoré môžu ovplyvniť klinické výsledky ochorenia COVID{24}}, je naša otázka stále platná pri definovaní, či PTX3 môže byť užitočným prognostickým faktorom na monitorovanie závažnosti ochorenia a úmrtnosti. V skutočnosti, hoci sa už predtým preukázalo, že hladiny cirkulujúceho PTX3 predstavovali nevýznamný rozdiel medzi pacientmi s COVID{28}} na JIS a bez JIS [44], zdá sa, že ich korelácia so smrťou súvisiacou s PTX{31}} celkom iné, čo potvrdzujú aj naše výsledky. Berúc do úvahy porovnateľnú úroveň komorbidity medzi týmito dvoma skupinami vo väčšine zahrnutých štúdií, trváme na tom, že budúce klinické hodnotenia by mali skúmať možné vzájomné imunozápalové presluchy vyvolané PTX, ktoré by sa mohli líšiť medzi pacientmi na JIS a pacientmi bez JIS. Medzitým naše zistenia prispievajú ku klinickému prehľadu o úlohe PTX3 v nepriaznivých výsledkoch COVID{36}}, a tiež podporujú potenciálne výhody imunoterapeutického prístupu pre pacientov s COVID-19 podobným tomu, ktorý bol predtým vystavený v onkológii pole [45].

cistanche tubulosa - zlepšenie imunitného systému
4. Závery
Celkovo možno povedať, že údaje diskutované v tomto systematickom prehľade a skúmané v metaanalýze zdôrazňujú PTX3 ako spoľahlivý biomarker pri predpovedaní úmrtia súvisiaceho s COVID{2}}. V 12 vhodných záznamoch bola vysoká expresia tohto proteínu prediktorom zlých klinických výsledkov, ktoré často korelovali s prijatím na JIS. Analýzou úmrtia súvisiaceho s PTX3- pomocou kvantitatívnej metódy sme zistili silnú štatistickú významnosť na JIS v porovnaní s pacientmi na všeobecnom oddelení (p=0,006). Vzhľadom na dôležitosť PTX3 pri riadení včasnej imunozápalovej reakcie vedúcej k závažnejšej forme ochorenia COVID-19 by lekári mali dôrazne odporúčať jeho analýzu laboratórnymi testami. Budúci výskum by mohol hlboko charakterizovať tento biomarker v rôznych klinických obrázkoch COVID-19 vyhodnotením rodových rozdielov a patofyziologických premenných spolu s krížovými rozhovormi o imunozápalovej signalizácii. Na záver možno povedať, že zozbierané dôkazy podporili vývoj liekových terapií zameraných na PTX{11}} ako sľubného prístupu na zmiernenie zápalovej reakcie u pacientov s COVID{12}}.
Referencie
1. Zhu, N.; Zhang, D.; Wang, W.; Li, X.; Yang, B.; Song, J.; Zhao, X.; Huang, B.; Shi, W.; Lu, R.; a kol. Nový koronavírus od pacientov s pneumóniou v Číne, 2019. N. Engl. J. Med. 2020, 382, 727–733. [CrossRef] [PubMed]
2. Harcourt, J.; Tamin, A.; Lu, X.; Kamili, S.; Sakthivel, SK; Murray, J.; Queen, K.; Tao, Y.; Paden, ČR; Zhang, J.; a kol. Izolácia a charakterizácia SARS-CoV-2 od prvého pacienta s COVID-19 v USA. bioRxiv 2020. [CrossRef]
3. Zheng, J. SARS-CoV-2: Objavujúci sa koronavírus, ktorý spôsobuje globálnu hrozbu. Int. J. Biol. Sci. 2020, 16, 1678–1685. [CrossRef] [PubMed]
4. Guo, YR; Cao, QD; Hong, ZS; Tan, YY; Chen, SD; Jin, HJ; Tan, KS; Wang, DY; Yan, Y. Pôvod, prenos a klinické terapie prepuknutia koronavírusovej choroby 2019 (COVID-19) – aktualizácia stavu. Mil. Med. Res. 2020, 7, 11. [CrossRef]
5. Li, LQ; Huang, T.; Wang, YQ; Wang, ZP; Liang, Y.; Huang, TB; Zhang, HY; Sun, W.; Wang, Y. Klinické charakteristiky pacientov s COVID{1}}, miera prepúšťania a miera úmrtnosti metaanalýzy. J. Med. Virol. 2020, 92, 577–583. [CrossRef]
6. Zheng, C.; Shao, W.; Chen, X.; Zhang, B.; Wang, G.; Zhang, W. Účinnosť vakcín proti COVID-19 v reálnom svete: prehľad literatúry a metaanalýza. Int. J. Infect. Dis. 2022, 114, 252–260. [CrossRef]
7. Forchette, L.; Sebastian, W.; Liu, T. Komplexný prehľad virológie COVID{1}}, vakcín, variantov a terapeutík. Curr. Med. Sci. 2021, 41, 1037–1051. [CrossRef]
8. Garlanda, C.; Bottazzi, B.; Magrini, E.; Inforzato, A.; Mantovani, A. PTX3, molekula na rozpoznávanie humorných vzorov, vo vrodenej imunite, oprave tkaniva a rakovine. Physiol. 2018, 98, 623–639. [CrossRef]
9. Bottazzi, B.; Doni, A.; Garlanda, C.; Mantovani, A. Integrovaný pohľad na humorálnu vrodenú imunitu: Pentraxíny ako paradigma. Annu. Rev. Immunol. 2010, 28, 157–183. [CrossRef]
10. Pepys, MB The Pentraxins 1975–2018: Serendipity, Diagnostics and Drugs. Predné. Immunol. 2018, 9, 2382. [CrossRef]
11. Magrini, E.; Mantovani, A.; Garlanda, C. Dvojitá komplexnosť PTX3 v zdraví a chorobe: Zákon o vyrovnávaní? Trends Mol. Med. 2016, 22, 497–510. [CrossRef] [PubMed]
12. Porte, R.; Davoudian, S.; Asgari, F.; Parente, R.; Mantovani, A.; Garlanda, C.; Bottazzi, B. Dlhý pentraxín PTX3 ako funkčný hráč s humornou vrodenou imunitou a biomarker infekcií a sepsy. Predné. Immunol. 2019, 10, 794. [CrossRef] [PubMed]
13. Garlanda, C.; Bottazzi, B.; Bastone, A.; Mantovani, A. Pentraxíny na križovatke medzi vrodenou imunitou, zápalom, ukladaním matrice a ženskou plodnosťou. Annu. Rev. Immunol. 2005, 23, 337-366. [CrossRef] [PubMed]
14. Daigo, K.; Mantovani, A.; Bottazzi, B. Jin-jang dlhého pentraxínu PTX3 pri zápale a imunite. Immunol. Lett. 2014, 161, 38–43. [CrossRef]
15. Caironi, P.; Masson, S.; Mauri, T.; Bottazzi, B.; Leone, R.; Magnoli, M.; Barlera, S.; Mamprin, F.; Fedele, A.; Mantovani, A.; a kol. Pentraxín 3 u pacientov s ťažkou sepsou alebo šokom: štúdia ALBIOS. Eur. J. Clin. Vyšetrovať. 2017, 47, 73–83. [CrossRef]
16. Jenny, NS; Arnold, AM; Kuller, LH; Tracy, RP; Psaty, BM Asociácie pentraxínu 3 s kardiovaskulárnym ochorením a smrťou zo všetkých príčin: The Cardiovascular Health Study. Arterioskler. Thromb. Vasc. Biol. 2009, 29, 594–599. [CrossRef]
17. Ramirez, GA; Rovere-Querini, P.; Blasi, M.; Sartorelli, S.; Di Chio, MC; Baldini, M.; De Lorenzo, R.; Bozzolo, EP; Leone, R.; Mantovani, A.; a kol. PTX3 zachytáva vaskulárny zápal pri systémových ochoreniach sprostredkovaných imunitou. Predné. Immunol. 2019, 10, 1135. [CrossRef]
18. Tiyo, BT; Schmitz, GJH; Ortega, MM; da Silva, LT; de Almeida, A.; Oshiro, TM; Duarte, A. Čo sa stane s imunitným systémom po očkovaní alebo zotavení z COVID-19? Life 2021, 11, 1152. [CrossRef]
19. Dan, JM; Mateus, J.; Kato, Y.; Hastie, KM; Yu, ED; Faliti, CE; Grifoni, A.; Ramirez, SI; Haupt, S.; Frazier, A.; a kol. Imunologická pamäť na SARS-CoV-2 hodnotená až 8 mesiacov po infekcii. Veda 2021, 371, eabf4063. [CrossRef] 20. Zuo, J.; Dowell, AC; Pearce, H.; Verma, K.; Long, HM; Begum, J.; Aiano, F.; Amin-Chowdhury, Z.; Hoschler, K.; Brooks, T.; a kol. Robustná T bunková imunita špecifická pre SARS-CoV{10}} sa udržiava 6 mesiacov po primárnej infekcii. Nat. Immunol. 2021, 22, 620–626. [CrossRef]
21. Turner, JS; Kim, W.; Kalaidina, E.; Goss, CW; Rauseo, AM; Schmitz, AJ; Hansen, L.; Haile, A.; Klebert, MK; Pusic, I.; a kol. Infekcia SARS-CoV-2 indukuje u ľudí dlhoveké plazmatické bunky kostnej drene. Príroda 2021, 595, 421–425. [CrossRef] [PubMed]
22. Wiech, M.; Chroscicki, P.; Swatler, J.; Stepník, D.; De Biasi, S.; Hampel, M.; Brewinska-Olchowik, M.; Maliszewska, A.; Sklinda, K.; Ďurlík, M.; a kol. Remodelácia dynamiky T-buniek počas dlhého obdobia COVID závisí od závažnosti infekcie SARS-CoV-2. Predné. Immunol. 2022, 13, 886431. [CrossRef] [PubMed]
23. Raveendran, AV; Jayadevan, R.; Sashidharan, S. Long COVID: Prehľad. Diabetes Metab. Syndr. 2021, 15, 869–875. [CrossRef] [PubMed]
24. Margiana, R.; Sharma, SK; Khan, BI; Alameri, AA; Opulencia, MJC; Hammid, AT; Hamza, TA; Babakulov, SK; Abdelbasset, WK; Jawhar, ZH Patogenita COVID-19 a úloha pentraxínu-3: Aktualizovaná prehľadová štúdia. Pathol. Res. Prax. 2022, 238, 154128. [CrossRef]
25. Ardizzone, A.; Capra, AP; Mondello, S.; Briuglia, S.; La Rosa, MA; Campolo, M.; Esposito, E. H1299R Variant vo faktore V a opakovaná strata tehotenstva: Systematic Review and Meta-Analysis Protocol. Gény 2022, 13, 1019. [CrossRef]
26. Capra, AP; Ardizzone, A.; Briuglia, S.; La Rosa, MA; Mondello, S.; Campolo, M.; Esposito, E. Systematický prehľad a metaanalýza asociácie medzi variantom FV H1299R a rizikom opakovanej straty tehotenstva. Biológia 2022, 11, 1608. [CrossRef]
27. Assandri, R.; Acordino, S.; Canetta, C.; Buscarini, E.; Scartabellati, A.; Tolassi, C.; Serana, F. Long pentraxin 3 ako marker závažnosti COVID-19: Dôkazy a perspektívy. Biochem. Med. 2022, 32, 020901. [CrossRef]
28. Brunetta, E.; Folci, M.; Bottazzi, B.; De Santis, M.; Gritti, G.; Protti, A.; Mapelli, SN; Bonovas, S.; Piovani, D.; Leone, R.; a kol. Expresia makrofágov a prognostický význam dlhého pentraxínu PTX3 v COVID-19. Nat. Immunol. 2021, 22, 19–24. [CrossRef]
29. de Bruin, S.; Bos, LD; van Roon, MA; Tuip-de Boer, AM; Schuurman, AR; Koel-Simmelinck, MJA; Bogaard, HJ; Tuinman, PR; van Agtmael, MA; Hamann, J.; a kol. Klinické znaky a prognostické faktory pri Covid-19: prospektívna kohortová štúdia. EBioMedicine 2021, 67, 103378. [CrossRef]
30. Feitosa, TA; Sa, MVDS; Pereira, VC; Cavalcante, MKDA; Pereira, VRA; da Costa Armstrong, A.; do Carmo, RF Asociácia polymorfizmov dlhého pentraxínu 3 a jeho plazmatické hladiny so závažnosťou COVID-19. Clin. Exp. Med. 2022, 1.–9. [CrossRef]
31. Genc, AB; Yaylaci, S.; Dheir, H.; Genc, AC; Issever, K.; Cekic, D.; Kocayigit, H.; Cokluk, E.; Karacan, A.; Sekeroglu, MR; a kol. Prediktívna a diagnostická presnosť dlhého pentraxínu-3 pri COVID-19 pneumónii. Turek. J. Med. Sci. 2021, 51, 448–453. [CrossRef] [PubMed]
32. Gutmann, C.; Takov, K.; Burnap, SA; Singh, B.; Ali, H.; Theofilatos, K.; Reed, E.; Hasman, M.; Nabeebaccus, A.; Fish, M.; a kol. SARS-CoV-2 RNAémia a proteomické trajektórie informujú o prognóze u pacientov s COVID-19 prijatých na intenzívnu starostlivosť. Nat. komun. 2021, 12, 3406. [CrossRef] [PubMed]
33. Hansen, CB; Sandholdt, H.; Moller, MEE; Perez-Alos, L.; Pedersen, L.; Israelsen, SB; Garred, P.; Benfield, T. Predikcia respiračného zlyhania a úmrtnosti u pacientov s COVID-19 používajúcich dlhý pentraxín PTX3. J. Innate Immun. 2022, 14, 493–501. [CrossRef] [PubMed]
34. Kukla, M.; Menzyk, T.; Dembinski, M.; Winiarski, M.; Garlicki, A.; Bociaga-Jašík, M.; Skonieczna, M.; Hudy, D.; Maziarz, B.; Kušnierz-Cabala, B.; a kol. Nedostatok fetuínu-A, ale nie pentraxín 3, FGF-21 alebo irisín, predisponuje k závažnejšiemu kurzu COVID-19. Biomolekuly 2021, 11, 1422. [CrossRef]
35. Kušnierz-Cabala, B.; Maziarz, B.; Dumnička, P.; Dembinski, M.; Kapusta, M.; Bociaga-Jašík, M.; Winiarski, M.; Garlicki, A.; Grodzicki, T.; Kukla, M. Diagnostický význam sérového galektínu-3 u hospitalizovaných pacientov s COVID-19 – predbežná štúdia. Biomolekuly 2021, 11, 1136. [CrossRef]
36. Lapadula, G.; Leone, R.; Bernasconi, DP; Biondi, A.; Rossi, E.; D'Angio, M.; Bottazzi, B.; Bettini, LR; Beretta, I.; Garlanda, C.; a kol. Hladiny dlhého pentraxínu 3 (PTX3) predpovedajú smrť, intubáciu a trombotické príhody u hospitalizovaných pacientov s COVID-19. Predné. Immunol. 2022, 13, 933960. [CrossRef]
37. Moulana, Z.; Bagherzadeh, M.; Mirzakhani, M.; Rostami, A.; Mohammadnia-Afrouzi, M.; Shahbazi, M. Zvýšené hladiny sérového pentraxínu 3 u pacientov s kritickým koronavírusovým ochorením-2019. Environ. Sci. Pollut. Res. Int. 2022, 29, 85569–85573. [CrossRef]
38. Sulička-Grodzička, J.; Surdacki, A.; Surmiak, M.; Sanák, M.; Wizner, B.; Sydor, W.; Bociaga-Jašík, M.; Strach, M.; Korkosz, M.; Skladaný, Ľ.; a kol. Chemerin ako potenciálny marker riešenia zápalu pri infekcii COVID-19. Biomedicína 2022, 10, 2462. [CrossRef]
39. Rothan, HA; Byrareddy, SN Epidemiológia a patogenéza epidémie koronavírusového ochorenia (COVID-19). J. Autoimmun. 2020, 109, 102433. [CrossRef]
40. Hu, B.; Huang, S.; Yin, L. Cytokínová búrka a COVID-19. J. Med. Virol. 2021, 93, 250–256. [CrossRef]
41. Gupta, A.; Madhavan, MV; Sehgal, K.; Nair, N.; Mahajan, S.; Sehrawat, TS; Bikdeli, B.; Ahluwalia, N.; Ausiello, JC; Wan, EY; a kol. Mimopľúcne prejavy COVID-19. Nat. Med. 2020, 26, 1017–1032. [CrossRef] [PubMed]
42. Rahman, S.; Montero, MTV; Rowe, K.; Kirton, R.; Kunik, F., Jr. Epidemiológia, patogenéza, klinické prejavy, diagnostika a liečba COVID-19: Prehľad súčasných dôkazov. Expert Rev. Clin. Pharmacol. 2021, 14, 601–621. [CrossRef] [PubMed]
43. Castanares-Zapatero, D.; Chalon, P.; Kohn, L.; Dauvrin, M.; Detollenaere, J.; de Noordhout, CM; Primus-de Jong, C.; Cleemput, I.; Van den Heede, K. Patofyziológia a mechanizmus dlhého COVID: Komplexný prehľad. Ann. Med. 2022, 54, 1473–1487. [CrossRef] [PubMed]
44. Ke, Y.; Wu, K.; Shen, C.; Zhu, Y.; Xu, C; Li, Q.; Hu, J.; Liu, S. Klinická užitočnosť cirkulujúceho pentraxínu 3 ako prognostického biomarkera pri koronavírusovej chorobe 2019: Systematický prehľad a metaanalýza. Infikovať. Dis. Ther. 2023, 12, 67–80. [CrossRef]
45. Zhou, Z.; Zhou, X.; Yang, Y.; Wang, L.; Wu, Z. Pan-Cancer Analysis of Pentraxin 3: A Potential Biomarker of COVID-19. Cancers 2022, 14, 4438. [CrossRef] [PubMed]
