Časť Ⅰ Vodík: Nová stratégia liečby ochorení obličiek
May 23, 2023
Abstraktné
1. pozadie
Vodík je chemická látka, ktorá sa v medicíne zatiaľ široko nepoužíva. Nedávne dôkazy však naznačujú, že vodík má mnohostranné farmakologické účinky, ako sú antioxidačné, protizápalové a antiapoptotické vlastnosti. Uskutočňuje sa zvýšený počet štúdií o aplikácii vodíka pri rôznych ochoreniach, najmä tých, ktoré postihujú obličkový systém.
2. zhrnutie
Vodík sa môže inhalovať ako plyn alebo kvapalina a môže sa podávať orálne, intravenózne alebo lokálne. Vodík môže rýchlo vstúpiť do suborganel, ako sú mitochondrie a jadro, jednoduchou difúziou, produkovať reaktívne formy kyslíka (ROS) a spúšťať poškodenie DNA. Vodík môže selektívne zachytávať hydroxylové radikály (•OH) a peroxynitrit (ONOO−), ale nie iné reaktívne kyslíkové radikály s fyziologickými funkciami, ako je peroxy anión (O2-) a peroxid vodíka (H2O2). Hoci sa potvrdil regulačný účinok vodíka na dráhu prenosu signálu, špecifický mechanizmus jeho vplyvu na signálne molekuly zostáva neznámy. Hoci mnohé štúdie skúmali terapeutické a preventívne účinky H2v bunkových a zvieracích experimentoch je klinických skúšok málo a stále veľmi zaostávajú. V dôsledku toho je potrebných viac klinických skúšok na preskúmanie úlohy vodíka pri ochorení obličiek, ako aj vplyvu jeho dávky, načasovania a formy na celkovú účinnosť. Pred použitím vodíka na liečbu ochorení obličiek budú potrebné rozsiahle randomizované kontrolované klinické štúdie.
3. Kľúčové správy
Tento článok prináša prehľad mechanizmov vodíka v liečbe obličkových ochorení a skúma možnosti jeho využitia v klinickej praxi.
Kľúčové slová
vodík; Ochorenie obličiek; Protizápalové; antioxidant; Bunková smrť.

Pre získanie kliknite semvýhody Cistanche
Úvod
Ochorenie obličiek je jednou z najčastejších chorôb u ľudí. Bežné typy ochorení obličiek zahŕňajú akútne poškodenie obličiek (AKI), renálnu fibrózu, polycystické ochorenie obličiek a karcinóm obličkových buniek. Existuje veľa možností liečby ochorení obličiek, vrátane liekovej terapie, dialýzy obličiek a transplantácie obličky. V posledných rokoch sa čoraz väčšia pozornosť venuje výskumu využívaniu vodíka na liečbu týchto ochorení. Vodík má silné redukčné vlastnosti a často sa používa ako redukčné činidlo pri chemických reakciách.
Terapeutické aplikácie H2boli prvýkrát ohlásené v roku 1975, keď sa veľkosť nádorov výrazne zmenšila, keď boli bezsrsté albínske myši so skvamocelulárnym karcinómom vystavené zmesi 2,5 percenta kyslíka a 97,5 percenta vodíka pri celkovom tlaku 8 atmosfér po dobu až 2 týždňov [1]. V roku 2007 Ohsawa a spol. [2] prvýkrát navrhli, že plynný vodík má antioxidačné a antiapoptotické vlastnosti, ktoré môžu chrániť mozog pred ischemicko-reperfúznymi (I/R) poraneniami (IRI) a mŕtvicou selektívnou neutralizáciou hydroxylových radikálov. Vodík pritiahol veľkú pozornosť kvôli jeho potenciálnemu terapeutickému účinku na ochorenia obličiek. Mnohé klinické a experimentálne modely ochorenia obličiek, ako aj hromadiace sa dôkazy v iných biomedicínskych doménach, preukázali, že vodík môže pôsobiť ako zachytávacie činidlo na selektívne zmiernenie reaktívnych foriem kyslíka (ROS). Inhalácia plynného vodíka alebo použitie vodného roztoku obsahujúceho vodík môže mať silný bunkový ochranný účinok.
V tomto prehľade sa zameriame na fyziologické úlohy vodíka pri ochoreniach obličiek, jeho potenciál ako terapeutickej stratégie a mechanizmy, ktoré sa môžu podieľať na jeho ochranných účinkoch. Okrem toho sa diskutuje o zisteniach nedávnych štúdií o vodíku v rôznych modeloch ochorenia obličiek.

Akčné mechanizmy
Plne vysvetliť preventívne a terapeutické účinky H21 a 2 ukazujú biologické účinky H2 a jeho vplyv na bunkovú smrť.
Biologické účinky H2
1. Antioxidácia
H2, silný oxidant, môže reagovať s nukleovými kyselinami bez rozdielu. Proces rozkladu látok a uvoľňovania energie v tele alebo mimo neho je známy ako oxidácia. Intenzívna oxidácia intracelulárnych ROS alebo voľných radikálov spôsobuje oxidačný stres (OS), stav nerovnováhy medzi oxidačnými a antioxidačnými účinkami v tele, ktorý sa považuje za hlavný prispievateľ k starnutiu a nástupu a progresii ochorenia. Akútny OS indukovaný I/R alebo zápalom spôsobuje vážne poškodenie tkanív a chronický OS je uznávaný ako príčinný činiteľ mnohých ochorení obličiek. Vodík dokáže zachytávať voľné radikály. Vodík selektívne redukuje hydroxylové radikály (•OH) a peroxydusitany (ONOO−), čo sú silné oxidanty, ktoré bez rozdielu reagujú s nukleovými kyselinami, lipidmi a proteínmi, čo vedie k fragmentácii DNA, peroxidácii lipidov a inaktivácii proteínov [2]. Potenciálne terapeutické prínosy H2boli prvýkrát opísané v roku 2007. Ohsawa et al. [2] zistil, že H2selektívne redukovali •OH a ONOO− v kultivovaných bunkách a skúmali, či H2 redukovali oxidované formy biomolekúl zapojených do metabolických oxidačno-redukčných reakcií v bezbunkových testoch. Pri izbovej teplote a neutrálnom pH roztoky nasýtené H2 nezredukovali oxidované formy nikotínamidadeníndinukleotidu, oxidovanú formu flavínadeníndinukleotidu alebo oxidovanú formu cytochrómu C.2neovplyvnil oxidačno-redukčný metabolizmus ani hladiny O2 −, H2O2a NO, z ktorých všetky hrajú pri nízkych koncentráciách dôležité fyziologické úlohy. Ako regulačné signálne molekuly sa podieľajú na mnohých kaskádach prenosu signálu a regulujú biologické procesy, ako je apoptóza, bunková proliferácia a diferenciácia. H2 má teda selektívne antioxidačné vlastnosti, ktoré chránia mozog pred poškodením I/R špecifickou neutralizáciou •OH a ONOO−, ale nie O2 −, H2O2a NO [2]. Na rozdiel od mnohých silne redukujúcich antioxidantov neovplyvňuje základné fyziologické procesy organizmu [3]. Okrem priamej neutralizácie voľných radikálov môže vodík aktivovať dráhu Nrf2/ARE in vivo a in vitro, čím zvyšuje transkripciu downstream génov antioxidačných enzýmov, ako je hemoxygenáza 1 (HO-1), a prispieva k tvorbe antioxidantov. činnosť [4]. Vodík môže tiež zvýšiť expresiu endogénnej superoxiddismutázy, katalázy [5] a redukovaného glutatiónu (GSH) [6], ktoré všetky pomáhajú znižovať oxidačné poškodenie. Vodík hrá rôzne úlohy pri selektívnom zachytávaní ROS, downstream kaskádovej signálnej transdukcii a regulácii aktivity antioxidačných enzýmov. Preto štúdie o antioxidačných mechanizmoch vodíka a jeho vplyve na znižovanie poškodenia spôsobeného OS v obličkách poskytujú nový smer pre budúcu liečbu ochorení obličiek.
2. Imunitný systém
Základné a klinické štúdie ukázali, že H2je dôležitým regulátorom s antioxidačnými, protizápalovými a antiapoptotickými účinkami [7]. H2ukázali, že majú protizápalový účinok v LPS-aktivovaných makrofágoch, podľa Hong et al. [8], inhibíciou uvoľňovania prozápalových cytokínov a zvýšením uvoľňovania protizápalových cytokínov, ktoré by mohlo byť sprostredkované HO-1. Následne niektorí výskumníci zistili, že resuscitácia pomocou fyziologického roztoku obohateného vodíkom by mohla výrazne zlepšiť poškodenie tkaniva a orgánov, potenciálne znížiť zápalové reakcie a OS inhibíciou expresie a aktivácie NF-κB [9]. H2bol tiež schopný inhibovať expresiu prozápalových cytokínov počas zápalu a znížiť skorú nadmernú expresiu prozápalových cytokínov, ako je interleukín (IL)- 1 , IL-6, IL-8 IL-10 a tumor nekrotizujúci faktor alfa (TNF- ) na mnohých zvieracích modeloch [10]. Sieť zápalových mediátorov a zápalových efektorových buniek a nerovnováha medzi prozápalovými cytokínmi a protizápalovými cytokínmi hrá dôležitú úlohu pri výskyte a progresii ochorení obličiek. Liečba zápalových ochorení obličiek z pohľadu prozápalových cytokínov a protizápalových cytokínov teda môže byť zaujímavou cestou pre ďalšie skúmanie úlohy vodíka pri regulácii a udržiavaní homeostázy pri zápalovom ochorení obličiek.
Diabetická nefropatia (DN) je závažnou komplikáciou diabetes mellitus. Metabolické poruchy sa môžu vyskytnúť pri DN a prejaviť sa ako lokálny zápal obličiek, ktorý môže viesť k fibróze a štrukturálnej prestavbe orgánu. Preto je riešenie imunitne sprostredkovaného zápalu veľmi dôležité pre liečbu DN [11]. Pri AKI, ako je infarkt renálnej artérie alebo poškodenie obličiek sprostredkované toxínmi, sa aktivujú imunitné bunky v obličkách. Poškodené renálne epitelové bunky aktivujú dráhy stresovej reakcie, čo vedie k sekrécii cytokínov a vazoaktívnych faktorov, čo vedie k imunopatologickému poškodeniu [12]. Vodík na druhej strane môže potlačiť tvorbu imunoreaktívnych látok [13]. Predpokladáme, že vodík má budúcnosť pri imunologickom ochorení obličiek, keďže je úzko spojený s významnými antioxidačnými účinkami. V súčasnosti však neexistujú žiadne klinické údaje, ktoré by to potvrdili. Na potvrdenie tejto teórie sú potrebné ďalšie štúdie.

Extrakt z cistanche a prášok z cistanche
3. Regulácia ER stresu
Stres endoplazmatického retikula (ER) nastáva, keď patologický stres indukuje akumuláciu rozložených proteínov v ER. Zhao a kol. [14] pozorovali, že inhalovaný vodík významne znížil hladiny proteínov súvisiacich so stresom ER a zmiernil poškodenie tkaniva pri IRI myokardu. Neskôr sa zistilo, že zmes H2a O2mohol inhibovať ER stres prostredníctvom ER-lokalizovaného eIF2 kinázy-eukaryotického iniciačného faktora 2 alfa-aktivujúceho transkripčný faktor 4 (PERK-eIF2 -ATF 4), enzýmu vyžadujúceho inozitol 1-X-box väzbový proteín 1 (IRE 1-XBP1) a ATF 6 dráh. Štúdia o vzťahu medzi H2a ER stres u potkanov s IRI zistili, že H2znížila expresiu GRP78 a faktora 2 spojeného s TNF receptorom [15], čo naznačuje, že ochranné účinky H2na IRI myokardu súvisia s poklesom stresu ER. Pokiaľ ide o ochorenie obličiek, štúdie zamerané na vplyv vodíka ako down-regulátora stresu ER sú zriedkavé; považujeme to však za zaujímavú budúcu líniu výskumu.
4. Kontrola kvality mitochondrií
Urátmi indukovaná dráha zápalu pri urátovej nefropatii zahŕňa vstup kryštálov urátov do intracelulárnych lyzozómov, ktoré sa rozkladajú za vzniku mitochondriálnych ROS, aktivujúcich zápaly NLRP3 [16]. Nadmerná produkcia ROS je spôsobená uvoľňovaním vápnika v ER, čo vedie k mitochondriálnej depolarizácii a strate potenciálu mitochondriálnej membrány. Mitochondriálna depolarizácia vedie k uvoľneniu väčšieho množstva ROS v mitochondriách. Negatívna regulácia ROS vodíkom môže pomôcť udržať mitochondriálnu funkciu [13, 17]. V súčasnosti ešte nebola zaznamenaná regulácia mitochondriálnej funkcie pomocou vodíka pri liečbe ochorení obličiek, ale toto by mohla byť sľubná oblasť výskumu.

Bylinka Cistanche
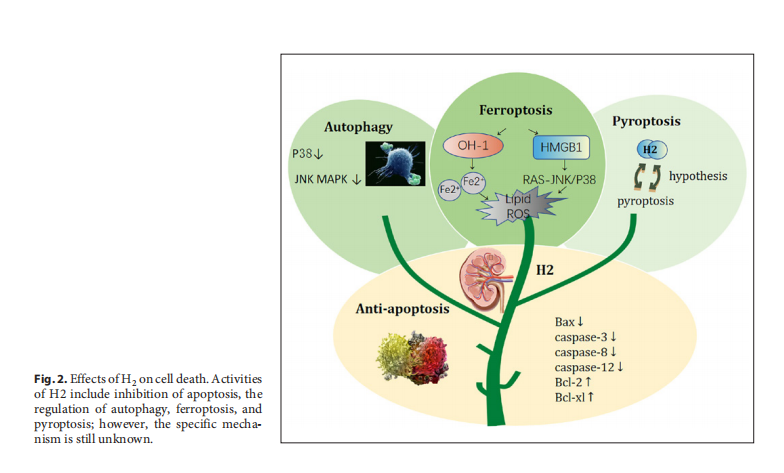
Účinky H2o bunkovej smrti
1. Anti-apoptóza
Apoptóza je forma programovanej bunkovej smrti charakterizovaná zmršťovaním buniek, tvorbou apoptotického tela, karyorexiou a kondenzáciou chromatínu. Apoptóza môže byť indukovaná endogénnymi aj exogénnymi cestami. H2hrá antiapoptotickú úlohu zvýšením alebo znížením regulácie faktorov súvisiacich s apoptózou. H2tiež inhibuje expresiu proapoptotických faktorov B-bunkového lymfómu - 2-asociovaného X-proteínu (Bax), kaspázy-3, -8 a -12 a zvyšuje reguláciu antiapoptotických faktorov B-bunkový lymfóm-2 (Bcl-2) a B-bunkový lymfóm-extra veľký (Bcl-xl) [18]. Zistilo sa, že intraperitoneálna injekcia roztoku bohatého na vodík 10 minút pred kostrovým svalstvom v I/R by mohla znížiť expresiu apoptotického proteínu Bax a cytochrómu C (ktorý môže aktivovať expresiu kaspázovej kaskádovej reakcie indukovanej kaspázou) a zvýšiť expresia antiapoptotického proteínu Bcl-2, čím sa zmierňuje poškodenie kostrového svalstva po reperfúzii [19]. Iní vedci zistili, že intraperitoneálna injekcia roztoku bohatého na vodík môže výrazne zvýšiť mieru prežitia kožných lalokov, čo súvisí s reguláciou dráhy ASK-1/JNK a pomeru Bax/Bcl{21}} [20]. Presný mechanizmus antiapoptotického účinku vodíka pri ochoreniach obličiek však nie je úplne jasný.
2. Autofágia
Autofágia je dôležitým mechanizmom na udržanie bunkovej homeostázy a podporuje využitie energie [21]. Autofágia má významný vplyv na funkciu obličiek a homeostázu. V štúdiách obličiek na dospelých zvieratách sa zistilo, že autofágia ovplyvňuje rôzne typy obličkových buniek, aby pomohla udržať patológiu obličiek a homeostázu [22]. Nadmerná autofágia alebo stres súvisiaci s autofágiou môže zhoršiť zápalové poškodenie tkanív a orgánov. Keď sa proteínové agregáty stanú toxickými, aktivuje sa autofágia a akonáhle nadmerná autofágia spôsobí poškodenie tkaniva, autofágia sa zablokuje. Zdá sa, že H2 hrá regulačnú úlohu [7]. Guan a spol. [23] odhalili, že H2 bol schopný zlepšiť poškodenie obličiek vyvolané chronickou intermitentnou hypoxiou (CIH) znížením stresu ER a aktiváciou autofágie inhibíciou aktivácie p38 a JNK MAPK závislej od OS. Na ďalšie preskúmanie základných mechanizmov sú však potrebné ďalšie štúdie na zvieratách a klinické štúdie.

účinky Cistanche
3. Pyroptóza
Definícia pyroptózy bola prvýkrát navrhnutá v roku 2012. Sprevádza ju akumulácia reaktívneho lipidového kyslíka katalyzovaná železom, bunková apoptóza, nekróza a autofágia [24]. V posledných rokoch sa preukázalo, že pyroptóza hrá dôležitú úlohu pri výskyte a rozvoji AKI [25, 26], renálnej fibróze [27], polycystickej chorobe obličiek [28] a karcinóme obličky [24, 29]. Pretože existuje značné prekrývanie medzi reguláciou vodíka a dráhami pyroptózy, predpokladali sme, že vodík by mohol hrať úlohu pri liečbe ochorení obličiek reguláciou dráh pyroptózy. Existuje len veľmi malý výskum v tejto veci, takže na potvrdenie tejto hypotézy môže byť potrebný ďalší výskum.
4. Ferroptóza
Ferroptóza je morfologicky, biochemicky a geneticky odlišná od apoptózy, autofágie a rôznych foriem nekrózy. Je charakterizovaná akumuláciou ROS a peroxidáciou lipidov závislou od železa a môže byť potlačená chelátormi železa, lipofilnými antioxidantmi a inhibítormi peroxidácie lipidov [24]. Nedávna štúdia [30] ukázala, že HMGB1 je nový regulátor ferroptózy prostredníctvom dráhy RAS-JNK/p38. Yu a spol. [31] preukázali, že liečba H2vo forme plynu znížili hladiny HMGB1. Preto predpokladáme, že H2môže byť potenciálnym liečivom pri ochoreniach obličiek. Ferroptóza je od železa závislá forma regulácie neapoptickej bunkovej smrti, ktorá prispieva k poškodeniu v modeloch AKI. HO-1, potenciálny zdroj intracelulárneho železa, je cytoprotektívny enzým indukovaný bunkovým stresom.
Pre svoje antiapoptotické a protizápalové vlastnosti [32] má ochranný účinok na AKI. Aktivita HO-1 môže byť zvýšená vodíkom. Nedávna štúdia [32] preukázala, že HO-1-deficitné obličkové epiteliálne bunky boli citlivejšie na feroptózu, čo naznačuje, že voľné železo produkované HO-1 nepodporuje samotnú ferroptózu a HO-1 má antiferroptózny účinok. Aj keď mechanizmy účinku vodíka na feroptózu musia byť ešte úplne objasnené, môže to pridať nové smery do hľadania liečby ochorení obličiek.
Referencie
1 Dole M, Wilson FR, Fife WP. Hyperbarická vodíková terapia: možná liečba rakoviny. Veda. 1975;190(4210):152–4.
2 Ohsawa I, Ishikawa M, Takahashi K, Watanabe M, Nishimaki K, Yamagata K a kol. Vodík pôsobí ako terapeutický antioxidant selektívnym znižovaním cytotoxických kyslíkových radikálov. Nat Med. 2007;13(6):688–94.
3 Ohta S. Nedávny pokrok smerom k vodíkovej medicíne: potenciál molekulárneho vodíka pre preventívne a terapeutické aplikácie. Curr Pharm Des. 2011;17(22):2241–52.
4 Xie Q, Li XX, Zhang P, Li JC, Cheng Y, Feng YL a kol. Plynný vodík chráni pred poškodením myokardu vyvolaným depriváciou séra a glukózy v bunkách H9c2 prostredníctvom aktivácie signálnej dráhy faktora 2/hémovej oxygenázy 1 súvisiaceho s NF-E{5}}. Mol Med Rep. 2014;10(2): 1143–9.
5 Wang F, Yu G, Liu SY, Li JB, Wang JF, Bo LL a kol. Fyziologický roztok bohatý na vodík chráni pred renálnym ischemickým/reperfúznym poškodením u potkanov. J Surg Res. 2011;167(2):e339–44.
6 Qian L, Cao F, Cui J, Huang Y, Zhou X, Liu S, a kol. Rádioprotektívny účinok vodíka v kultivovaných bunkách a myšiach. Free Radic Res. 2010; 44 (3): 275-82.
7 Huang CS, Kawamura T, Toyoda Y, Nakao A. Nedávne pokroky vo výskume vodíka ako terapeutického medicínskeho plynu. Free Radic Res. 2010; 44(9):971-82.
8 Chen HG, Xie KL, Han HZ, Wang WN, Liu DQ, Wang GL a kol. Heme oxygenáza-1 sprostredkúva protizápalový účinok molekulárneho vodíka v makrofágoch RAW 264.7 stimulovaných LPS. Int J Surg. 2013;11(10):1060–6.
9 Wang X, Yu P, Yang Y, Liu X, Jiang J, Liu D a kol. Resuscitácia fyziologickým roztokom bohatým na vodík zmierňuje zápal spôsobený ťažkými popáleninami s oneskorenou resuscitáciou. Popáleniny. 2015;41(2): 379–85.
10 Liu W, Shan LP, Dong XS, Liu XW, Ma T, Liu Z. Kombinovaná skorá tekutinová resuscitácia a inhalácia vodíka zmierňuje poškodenie pľúc a čreva. World J Gastroenterol. 2013; 19(4):492-502.
11 Zheng Z, Zheng F. Imunitné bunky a zápal pri diabetickej nefropatii. J Diabetes Res. 2016;2016:1841690.
12 Yatim KM, Lakkis FG. Krátka cesta imunitným systémom. Clin J Am Soc Nephrol. 2015;10(7):1274–81.
13 Yang M, Dong Y, He Q, Zhu P, Zhuang Q, Shen J a kol. Vodík: nová možnosť v liečbe ľudských chorôb. Oxid Med Cell Longev. 2020;2020:8384742.
14 Zhang Y, Liu Y, Zhang J. Nasýtený fyziologický roztok tlmí endotoxínmi indukovanú pľúcnu dysfunkciu. J Surg Res. 2015;198(1):41–9.
15 Huang T, Wang W, Tu C, Yang Z, Bramwell D, Sun X. Soľný roztok bohatý na vodík zmierňuje ischemicko-reperfúzne poškodenie v kostrovom svale. J Surg Res. 2015;194(2):471–80.
16 Liu YQ, Liu YF, Ma XM, Xiao YD, Wang YB, Zhang MZ a kol. Fyziologický roztok bohatý na vodík zmierňuje apoptózu vyvolanú ischémiou/reperfúziou kože prostredníctvom regulácie pomeru Bax/Bcl-2 a dráhy ASK- 1/JNK. J Plast Reconstr Aesthet Surg. 2015;68(7):e147–56.
17 Zhong H, Song R, Pang Q, Liu Y, Zhuang J, Chen Y a kol. Propofol inhibuje parthanatos prostredníctvom ROS-ER-kalcium-mitochondriálnej signálnej dráhy in vivo a in vitro. Cell Death Dis. 2018; 9 (10): 932.
18 Zhao YS, An JR, Yang S, Guan P, Yu FY, Li W, a kol. Zmes vodíka a kyslíka na zlepšenie srdcovej dysfunkcie a patologických zmien myokardu vyvolaných intermitentnou hypoxiou u potkanov. Oxid Med Cell Longev. 2019; 2019:7415212.
19 Gao Y, Yang H, Chi J, Xu Q, Zhao L, Yang W a kol. Plynný vodík zoslabuje ischemicko-reperfúzne poškodenie myokardu nezávisle od postkondicionovania u potkanov zoslabením autofágie vyvolanej stresom endoplazmatického retikula. Cell Physiol Biochem. 2017;43(4):1503–14.
20 Isaka Y, Takabatake Y, Takahashi A, Saitoh T, Yoshimori T. Hyperurikémiou indukované zápaly a ochorenia obličiek. Transplantácia nefrolového číselníka. 2016;31(6):890–6.
21 Parzych KR, Klionsky DJ. Prehľad autofágie: morfológia, mechanizmus a regulácia. Antioxidačný redoxný signál. 2014;20(3): 460–73.
22 He L, Livingston MJ, Dong Z. Autofágia pri akútnom poškodení a oprave obličiek. Nephron Clin Pract. 2014;127(1–4):56–60.
23 Guan P, Sun ZM, Luo LF, Zhou J, Yang S, Zhao YS a kol. Vodík chráni pred chronickou intermitentnou hypoxiou vyvolanou renálnou dysfunkciou podporou autofágie a zmiernením apoptózy. Life Sci. 2019;225:46–54.
24 Dixon SJ, Lemberg KM, Lamprecht MR, Skouta R, Zaitsev EM, Gleason CE, et al. Ferroptóza: forma neapoptickej bunkovej smrti závislá od železa. Bunka. 2012;149(5):1060–72.
25 Friedmann Angeli JP, Schneider M, Proneth B, Tyurina YY, Tyurin VA, Hammond VJ a kol. Inaktivácia regulátora feroptózy Gpx4 spúšťa akútne zlyhanie obličiek u myší. Nat Cell Biol. 2014;16(12):1180–91.
26 Müller T, Dewitz C, Schmitz J, Schröder AS, Bräsen JH, Stockwell BR, et al. Nekroptóza a ferroptóza sú alternatívne cesty bunkovej smrti, ktoré fungujú pri akútnom zlyhaní obličiek. Cell Mol Life Sci. 2017;74(19):3631–45.
27 Hou W, Xie Y, Song X, Sun X, Lotze MT, Zeh HJ 3rd, et al. Autofágia podporuje ferroptózu degradáciou feritínu. Autofágia. 2016; 12(8):1425-8.
28 Schreiber R, Buchholz B, Kraus A, Schley G, Scholz J, Ousingsawat J, et al. Peroxidácia lipidov riadi rast obličkových cýst in vitro prostredníctvom aktivácie TMEM16A. J Am Soc Nephrol. 2019;30(2):228–42.
29 Yang WS, SriRamaratnam R, Welsch ME, Shimada K, Skouta R, Viswanathan VS a kol. Regulácia smrti feroptózových rakovinových buniek pomocou GPX4. Bunka. 2014;156(1–2):317–31.
30 Ye F, Chai W, Xie M, Yang M, Yu Y, Cao L a kol. HMGB1 reguluje elastínom indukovanú feroptózu prostredníctvom signalizácie RAS-JNK/p38 v bunkách HL-60/NRAS(Q61L). Am J Cancer Res. 2019; 9(4):730-9.
31 Yu Y, Yang Y, Yang M, Wang C, Xie K, Yu Y. Plynný vodík znižuje uvoľňovanie HMGB1 v pľúcnych tkanivách septických myší v dráhe závislej od Nrf2/HO- 1-. Int Immunopharmacol. 2019;69:11–8.
32 Adedoyin O, Boddu R, Traylor A, Lever JM, Bolisetty S, George JF a kol. Hemová oxygenáza-1 zmierňuje feroptózu v bunkách proximálneho tubulu obličiek. Am J Physiol Renálny Physiol. 2018; 314(5):F702–14.
Bo WangaZhuoshu Lib, cLongfei MaodMingyi ZhaobBingchang YangeXiaowu TaoaYuxiang Lia Guangming Yina
oddelenie urológie, The Third Xiangya Hospital, Central South University, Changsha, Čína;
bKatedra pediatrie, The Third Xiangya Hospital, Central South University, Changsha, Čína;
c Xiangya School of Medicine, Central South University, Changsha, Čína;
d Bioinformatics Center, College of Biology, Hunan University, Changsha, Čína;
e Department of Critical Care Medicine, Central South University, Changsha, Čína
