Prvá časť Genetika ochorenia obličiek: Neočakávaná úloha zriedkavých porúch
Jun 09, 2023
Abstraktné
V súčasnosti sú známe stovky rôznych genetických príčin chronického ochorenia obličiek, a hoci sú individuálne zriedkavé, spolu sú významnými prispievateľmi k stavom dospelých aj detí. Tradičné genetické prístupy sa vo veľkej miere spoliehali na identifikáciu veľkých rodín s viacerými postihnutými členmi a boli základom pre identifikáciu genetických ochorení obličiek. So zvýšeným využívaním masívne paralelného sekvenovania a zlepšeniami imputácie genotypu môžeme analyzovať zriedkavé varianty vo veľkých kohortách nepríbuzných jednotlivcov, čo vedie k personalizovanej starostlivosti o pacienta a významnému pokroku vo výskume. Tento prehľad hodnotí prínos zriedkavých porúch k starostlivosti o pacienta a štúdiu genetických ochorení obličiek a zdôrazňuje kľúčové pokroky, ktoré využívajú nové techniky na zlepšenie našej schopnosti identifikovať nové asociácie génov a chorôb.
Kľúčové slová
genetické ochorenie obličiek, kolapsová analýza, presná medicína, masívne paralelné sekvenovanie, genomika, chronické ochorenie obličiek

Ak chcete vedieť, kliknite semaké sú výhody Cistanche
ÚVOD
Chronické ochorenie obličiek (CKD) je komplexný stav, ktorý zahŕňa mnoho individuálnych ochorení charakterizovaných abnormalitami v štruktúre alebo funkcii obličiek (1). Celosvetovo je ochorenie obličiek bežné, s odhadovanou prevalenciou 9 percent a je hlavným prispievateľom k morbidite a úmrtnosti (2). Podobne ako iné bežné ochorenia má CKD relatívne vysokú dedičnosť, pričom odhady dedičnosti v širokom zmysle sa pohybujú od 19 percent do 54 percent v závislosti od použitého biomarkera (3–5).
Genetic variation can be broadly dichotomized into common variants, present in more than 1% of the alleles of the population [a minor allele frequency (MAF) of >0.01] a zriedkavé varianty (MAF<0.01) (6–8). The role of common variants in kidney disease has been assessed using genome-wide association studies (GWAS), which have explained only 20% of an estimated 54% heritability in creatinine-based estimated glomerular filtration rate (4). On the other side of the spectrum, rare pathogenic variants are responsible for most Mendelian (monogenic) diseases. There are over 600 Mendelian forms of kidney disease, responsible for 50% of childhood-onset kidney disease; the majority of the causative variants are very rare or private within a specific family (9, 10). Although present at a lower frequency, Mendelian kidney diseases are identified in approximately 10% of adult patients, with the specific diagnostic yield of testing varying based on the individual's type of kidney disease, family history, age at onset, and extra-renal manifestations (11). Similar to pediatric cases, rare and private variants drive most diagnoses in adult cases. The data on the impact of rare disorders in CKD are now emerging and are consistent with analyses of other complex traits, which have demonstrated that a significant amount of missing heritability is explained by rare protein-altering variants that are not well captured by current genotyping and imputation techniques but can be analyzed using massively parallel sequencing of the exome (exome sequencing, ES) or genome (12, 13).
Zriedkavé varianty zapojené do ochorenia obličiek sa líšia svojou triedou, dedičnosťou, postihnutým génom a klinickým fenotypom. Napríklad zriedkavé štrukturálne varianty a variácie v počte kópií génu boli spojené s vývojom vrodených anomálií obličiek a močových ciest (CAKUT) a jednonukleotidové varianty a malé inzercie a delécie (indely) boli spojené s ochoreniami obličiek. naprieč fenotypovým spektrom (14, 15). Zriedkavé somatické varianty sa podieľajú ako druhý zásah do vývoja cýst pri autozomálne dominantnej polycystickej chorobe obličiek (ADPKD) a ako hnacie varianty pri klonálnej hematopoéze s neurčitým potenciálom (CHIP), nemalígnom stave súvisiacom s vekom, ktorý môže spôsobiť zvýšenú riziko zlyhania obličiek a komplikácií CKD (16, 17). Zriedkavé varianty mozaiky tiež ovplyvňujú závažnosť X-spojeného Alportovho syndrómu, čo naznačuje ďalšiu zložitosť pri určovaní účinku variantu (18).
V tomto prehľade popisujeme úlohu, ktorú zohrávajú zriedkavé varianty v genetike ochorenia obličiek. Skúmame ich ústredné miesto v diagnostických štúdiách, vrátane dôsledkov pre starostlivosť o pacienta a využitie genetického testovania v prognostike a liečbe. Potom preskúmame typické prístupy používané na identifikáciu a overenie nových zriedkavých variantných asociácií s ochorením. Záverom je skúmanie veľkých súborov údajov a integrácia klinických údajov z elektronických zdravotných záznamov, ktoré ponúkajú príležitosti na vyhodnotenie genetických účinkov v rozsahu, ktorý bol predtým nemožný.

Doplnky Cistanche
NASTAVENIA KLINICKEJ DIAGNOSTIKY
Genetické ochorenie obličiek je zastrešujúci pojem, ktorý zachytáva stovky zriedkavých porúch s identifikovanou genetickou príčinou. Doteraz bolo identifikovaných viac ako 600 monogénnych porúch s obličkovými a urologickými fenotypmi (obrázok 1) (19). Takmer všetky tieto genetické stavy sú pozorované u menej ako 1 z 2000 ľudí, ale kumulatívne predstavujú piatu najčastejšiu príčinu zlyhania obličiek (20). Zatiaľ čo niekoľko monogénnych porúch predstavuje veľkú časť prípadov, zvyšné prípady možno pripísať veľkému počtu zriedkavých porúch. Tento dlhý chvost v distribúcii monogénnych ochorení obličiek má dôležité dôsledky pre klinické diagnostické algoritmy a snahy o objavovanie génov. Uskutočnilo sa niekoľko diagnostických štúdií s cieľom lepšie definovať diagnostický výťažok a klinické dôsledky genetického testovania u rôznych populácií pacientov s ochorením obličiek. Jedným z kľúčových zistení v týchto štúdiách je, že väčšina identifikovaných patogénnych variantov je veľmi zriedkavá, s maximálnym (max.) MAF menej ako 1 × 10–4, alebo sú súkromné v rámci jednej rodiny.

1. Pediatrické stavy
Pôvodne sa predpokladalo, že genetické ochorenia sú prevažne detské, preto sa skoršie diagnostické štúdie zamerali na hodnotenie detských pacientov (11, 21). Jedna takáto štúdia použila ES na vyhodnotenie 187 pediatrických pacientov s nefrotickým syndrómom rezistentným na steroidy a identifikovala genetickú príčinu v 49 (26 percent) prípadoch a 77 diagnostických variantoch (22). Je zaujímavé, že napriek recesívnej dedičnosti týchto stavov boli všetky varianty extrémne zriedkavé; 32 (42 percent ) chýbalo v literatúre, 39 (51 percent ) chýbalo v Exome Aggregation Consortium (ExAC) a ďalších 25 (32 percent ) malo maximálny MAF menší ako 1 × 10- 4. Výnimkou je detský nefrotický syndróm rezistentný na steroidy spôsobený variantmi NPHS2, ktorý ponúka zaujímavý príklad interakcie bežných a zriedkavých variantov ochorenia. NPHS2 p.R229Q je najčastejšie identifikovaný patogénny variant v tejto populácii pacientov s maximálnym MAF v ExAC 0,029. Variant NPHS2 p.R229Q však nespôsobuje ochorenie, ak je prítomný v homozygotnom stave, a je patogénny iba vtedy, keď je spárovaný s niektorými inými zriedkavými variantmi NPHS2 (23). V citovanej štúdii boli škodlivé varianty nájdené v trans k NPHS2 p.R229Q u postihnutých jedincov vždy zriedkavé a často súkromné, pričom NPHS2 p.E264Q bol najbežnejší v ExAC s maximálnym MAF 0,003. Podobne hodnotenie genetických príčin CAKUT v 232 rodinách identifikovalo 32 rôznych príčinných variantov v 32 prípadoch (14 percent) postihujúcich 22 génov, pričom 16 (50 percent) z týchto variantov chýba v literatúre a 28 (88 percent) je veľmi zriedkavé alebo chýba. z databázy genómovej agregácie (gnomAD) (24).
2. Rozšírenie na dospelých pacientov
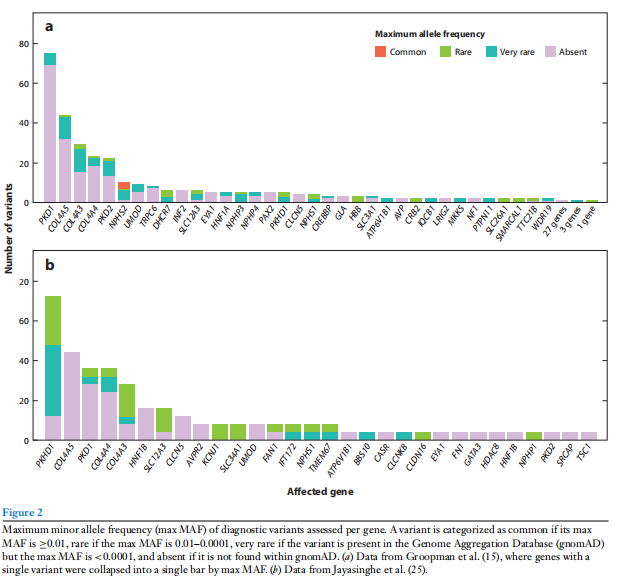
ES sa používa na vyhodnotenie rôznych populácií pacientov s ochorením obličiek vrátane jedincov s ochorením v dospelosti. Najväčšia štúdia, ktorá tak urobila, zahŕňala 3 315 jedincov s CKD z akejkoľvek príčiny, z ktorých 2 144 malo rozvinuté zlyhanie obličiek a 2 837 boli dospelí pri vstupe do štúdie (15). Táto štúdia identifikovala molekulárnu diagnózu u 307 jedincov (9,1 percenta), čo viedlo k diagnóze 66 rôznych mendelovských ochorení obličiek. Štúdia identifikovala 343 diagnostických variantov, z ktorých 340 99 percent ) je u gnomAD zriedkavé. Väčšina variantov bola buď veľmi zriedkavá, s maximálnym MAF menej ako 1 × 10-4 (n=84, 24 percent), alebo súkromná (n=229, 67 percent) (obrázok 2a).
3. Dopady genetickej diagnózy
Jedným z kľúčových zistení diagnostických štúdií je, že väčšina genetických diagnóz má priamy vplyv na starostlivosť o pacienta, aj keď je v súčasnosti k dispozícii obmedzený počet cielených liečebných postupov. Groopman a kol. (15) zistili, že genetická diagnóza viedla ku klinickému dopadu v 89 percentách prípadov, vrátane 76 percent prípadov, keď bolo pred testovaním podozrenie na genetické ochorenie obličiek. Tieto klinické vplyvy boli retrospektívne hodnotené a siahali od informujúcej prognózy až po zmenu rozhodnutí o transplantácii a liečbe. Dôležité je, že genetická diagnóza u pacientov s CKD neznámej etiológie objasnila príčinu ochorenia obličiek vo všetkých prípadoch, mala prognostické dôsledky pre 77 percent, iniciovala cielenú špecializovanú starostlivosť pre 77 percent a zmenila liečbu pre 62 percent. Prospektívne údaje podporujúce klinickú užitočnosť genetického testovania na ochorenie obličiek boli nedávno publikované u 204 pacientov s podozrením na genetické ochorenie obličiek, ktorí podstúpili ES. Priamy klinický dopad bol hlásený u 47 (59 percent) probandov s genetickou diagnózou a 73 (91 percent) rodín (25). Klinické vplyvy zahŕňali prevenciu 10 biopsií obličiek, zmeny liečebných plánov v 16 prípadoch a zmenený dohľad v 35 prípadoch, ktoré boli opäť poháňané zriedkavými variantmi (obrázok 2b).

Extrakt z cistanche
4. Prognóza
Variabilita v klinickom obraze genetických foriem ochorení obličiek skomplikovala poskytovanie prognostických informácií pacientom, aj keď je identifikovaná genetická príčina. Navyše väčšina patogénnych variantov spojených s ochorením obličiek je veľmi zriedkavá alebo súkromná v rámci rodiny, čo obmedzuje našu schopnosť poskytnúť prognózu založenú na jednotlivých variantoch. Napriek tomu sú korelácie genotyp-fenotyp súčasťou ľudskej genetiky od jej počiatkov, pričom sa často využívajú zovšeobecniteľné varianty charakteristík, ako je typ účinku na proteín, vlastnosti zmenenej aminokyseliny alebo poloha variantu v proteíne. V nefrológii sa dve najzrelšie aplikácie tohto prístupu zameriavajú na ADPKD a Alportov syndróm. Pre pacientov s ADPKD bol vyvinutý a overený systém hodnotenia PROPKD (predpovedanie renálnych výsledkov pri polycystickej chorobe obličiek) na predpovedanie priemerného veku jednotlivca pri zlyhaní obličiek integráciou klinických a variantných údajov (26). Skrátené varianty v PKD1 nesú najvyššie riziko zlyhania obličiek, po ktorých nasledujú neskrátené varianty PKD1, potom varianty v PKD2 a tiež sa zdá, že neskrátené inzercie a delécie v rámci v PKD1, ktoré menia dĺžku proteínu, nesú vyššie riziko ako missense varianty ( 27). Podobne pre pacientov s Alportovým syndrómom nesú nezmyselné varianty najzávažnejšiu prognózu, zatiaľ čo zostrihové a missense varianty predpovedajú stredné a mierne fenotypy. Iné faktory, ako je poloha variantu v géne, jeho poloha vo vzťahu k nekolagénnym prerušeniam a substitučná aminokyselina, majú tiež vplyv na prognózu pacienta (28–30). Budúce nástroje môžu zahŕňať aj prediktívne informácie z bežných aj zriedkavých variantov na zlepšenie ich výkonu (31). Dostupnosť väčších súborov údajov by umožnila integráciu viacerých variantov a ideálne odlišnejších rodín s rovnakými variantmi do vývoja robustných prognostických nástrojov, ktoré by umožnili lepšie predpovede. Takéto nástroje by mohli významne ovplyvniť klinické štúdie, pretože účastníci by mohli byť stratifikovaní na základe očakávanej progresie ich ochorenia.

Cistanche pilulky
5. Liečba
Diagnostické štúdie ukázali, že získanie genetickej diagnózy môže mať priamy vplyv na liečbu (tabuľka 1). Príklady zahŕňajú použitie suplementácie vysokými dávkami koenzýmu Q10 (CoQ10) u pacientov s nefrotickým syndrómom a diagnostické varianty v rámci dráhy CoQ10 (COQ2, COQ6, ADCK2/COQ8B, PDSS2, MTTL1) a použitie inhibítorov xantínoxidázy u pacientov s APRT nedostatok (adenín fosforibozyltransferázy) (32, 33). Genetická diagnóza môže obmedziť vystavenie neúčinným liečebným postupom; napríklad, keď sa identifikuje genetická príčina nefrotického syndrómu, imunosupresia sa zvyčajne nepoužíva, pretože väčšina prípadov genetického nefrotického syndrómu nereaguje a tieto liečby prinášajú značné riziká (34). Budúce štúdie by mali posúdiť výhody vyhýbania sa nepriaznivým účinkom, ako je zníženie rizika infekcie a rakoviny z obmedzenia imunosupresie v dôsledku genetického testovania. Okrem toho schopnosť odhaliť nediagnostikovaných pacientov s monogénnymi ochoreniami môže pomôcť pri stratifikácii rizika v klinických štúdiách s cieľom optimalizovať výkon a znížiť vystavenie vedľajším účinkom.

Konečným cieľom je vyvinúť liečebné postupy. Jedným z najpokročilejších príkladov v nefrológii je aplikácia génovej terapie Fabryho choroby (35). Fabryho choroba je spôsobená viac ako 1, 000 rôznymi variantmi v géne GLA, väčšinou veľmi zriedkavými alebo súkromnými, ktoré vedú k zníženej aktivite galaktozidázy A a akumulácii glykosfingolipidov (36). Štandardnou liečbou tohto ochorenia je enzymatická substitučná terapia (ERT), ktorá si vyžaduje pravidelné infúzie a môže viesť k vzniku protidrogových protilátok obmedzujúcich liečbu. V pilotnej štúdii bezpečnosti však päť mužov s klasickou Fabryho chorobou v dôsledku veľmi zriedkavých variantov missense, ktorí boli stabilne liečení ERT, bolo liečených génovou terapiou (35). Podstúpili lentivírusom sprostredkovanú génovú terapiu ex vivo, kde sa hematopoetické kmeňové/progenitorové bunky transdukovali funkčným génom GLA a potom sa znovu zaviedli prostredníctvom autológnej transplantácie hematopoetických kmeňových buniek. Títo pacienti preukázali trvalú normalizáciu aktivity leukocytovej galaktozidázy A a stabilné hladiny glykosfingolipidov, ktoré umožnili trom (60 percentám) z nich prerušiť ERT s primeraným profilom nežiaducich účinkov. Táto štúdia nám dáva nádej, že s ďalším zdokonaľovaním môže byť liečebná liečba dostupná pre viac našich pacientov.
Fabryho choroba tiež poskytuje ďalšie zaujímavé príklady personalizovanej terapie vrátane chaperónovej terapie a rozhodnutí o liečbe pre pacientky. Bežným mechanizmom ochorenia pri tomto stave je zmenený transport proteínov vedúci k zníženiu aktivity enzýmov. Migalastat je chaperónová molekula, ktorá obnovuje funkciu enzýmu a vykazuje klinickú účinnosť podobnú ERT u 35–50 percent jedincov s prístupným variantom, ale nemá žiadny účinok u jedincov s neprispôsobiteľnými variantmi (37, 38). Táto variantná špecifickosť robí z genetického testovania kľúčový krok pri optimalizácii terapie pre pacientov s Fabryho chorobou. Dlho sa predpokladalo, že v dôsledku X-viazanej povahy choroby boli ženy nepostihnutými prenášačmi; teraz je však jasné, že je postihnutých mnoho žien a že existuje komplexná súhra medzi špecifickými variantnými charakteristikami a skreslenou X inaktiváciou, ktorá vedie k vysoko heterogénnym klinickým prejavom (39). To skomplikovalo rozhodovanie o tom, kedy a ako liečiť pacientky s Fabryho chorobou, keďže niektorí jedinci majú prospech z terapie, ale chýbajú nám nástroje na predpovedanie odpovede skôr, ako sa u pacientov prejavia symptómy, čo poukazuje na oblasť, ktorá si vyžaduje ďalší výskum.

Cistanche prášok
Pre pacientov s genetickým ochorením obličiek sa stávajú dostupné ďalšie cielené terapie s použitím nových techník, ako je RNA interferencia (RNAi), antisense-oligonukleotidy (ASO) a CRISPR-Cas9. RNAi ukázal veľký prísľub na liečbu genetických ochorení obličiek s pozitívnymi štúdiami fázy III s použitím patisiranu na liečbu dedičnej transtyretínovej amyloidózy v dôsledku variantov TTR a lumasiranu na liečbu primárnej hyperoxalúrie typu 1 v dôsledku variantov AGT (40, 41). Tieto liečby boli navrhnuté tak, aby boli variantne agnostické, čo im umožňuje ich použitie na liečbu jedincov s množstvom rôznych zriedkavých variantov. CRISPR-Cas9 bol študovaný na malej skupine jedincov s transtyretínovou amyloidózou a ukázalo sa, že znižuje produkciu TTR v sére prostredníctvom cieleného génového knockdownu pomocou in vivo techniky podávania (42). Ukázalo sa, že liečba ASO s preskočením exónu skrátených variantov COL4A5 u myší vyvoláva klinické a histologické zlepšenia zmenou účinku proteínu na deléciu exónu v rámci (43). Môže sa to stať možnosťou liečby pre pacientov s rôznymi vzácnymi skrátenými variantmi COL4A5, ktoré zvyčajne spôsobujú závažné ochorenie, ale ešte sa musia študovať na ľuďoch. Terapeutické prístupy k nefropatii spojenej s APOL{16}} zahŕňajú použitie liečby ASO na zníženie expresie APOL1 a použitie inhibítorov APOL1 s malými molekulami na zníženie jeho funkcie (44). Tieto cielené a personalizované terapie budú pravdepodobne aplikované na rôzne genetické choroby a ponúkajú našim pacientom nádej na lepšiu liečbu v budúcnosti.
LITERATÚRA
1. Levin A, Stevens PE, Bilous RW a kol. 2013. Pracovná skupina CKD Choroba obličiek: Zlepšenie globálnych výsledkov (KDIGO). Usmernenie klinickej praxe KDIGO 2012 na hodnotenie a manažment chronického ochorenia obličiek. Kidney Int. Suppl. 3(1):1-150
2. Bikbov B, Purcell CA, Levey AS, a kol. 2020. Globálna, regionálna a národná záťaž chronickým ochorením obličiek, 1990–2017: systematická analýza pre štúdiu Global Burden of Disease 2017. Lancet 395(10225):709–33
3. Arpegård J, Viktorin A, Chang Z, a kol. 2015. Porovnanie dedičnosti odhadov funkcie obličiek na základe cystatínu C a kreatinínu a ich vzťah k dedičnosti kardiovaskulárnych ochorení. J. Am. Heart Assoc. 4(1):e001467
4. Wuttke M, Li Y, Li M a kol. 2019. Katalóg genetických lokusov spojených s funkciou obličiek z analýz milióna jedincov. Nat. Genet. 51(6):957-72
5. Zhang J, Thio CHL, Gansevoort RT, a kol. 2021. Familiárna agregácia CKD a dedičnosť obličkových biomarkerov vo všeobecnej populácii: Lifelines Cohort Study. Am. J. Kidney Dis. 77(6):869–78
6. Karczewski KJ, Francioli LC, Tiao G, a kol. 2020. Mutačné obmedzujúce spektrum kvantifikované z variácií u 141 456 ľudí. Nature 581 (7809): 434–43
7. Lek M, Karczewski KJ, Minikel EV, et al. 2016. Analýza genetickej variácie kódujúcej proteín u 60 706 ľudí. Nature 536(7616):285–91
8. The 1000 Genomes Proj. Manželka. 2015. Globálna referencia pre ľudské genetické variácie. Nature 526 (7571): 68–74
9. Ars E, Ballarin J, Ruiz P a kol. 2011. Klinická užitočnosť genetického testovania u detí a dospelých s nefrotickým syndrómom rezistentným na steroidy. Clin. J. Am. Soc. Nephrol. 6(5):1139-48
10. Wühl E, van Stralen KJ, Wanner C, a kol. 2014. Renálna substitučná liečba zriedkavých ochorení postihujúcich obličky: analýza registra ERA-EDTA. Nephrol. Dialyzačná transplantácia. 29(doplnok 4):iv1–8
11. Cocchi E, Nestor JG, Gharavi AG. 2020. Klinický genetický skríning u dospelých pacientov s ochorením obličiek. Clin. J. Am. Soc. Nephrol. 15(10):1497-510
12. Génin E. 2020. Chýbajúca dedičnosť komplexných chorôb: prípad vyriešený? Hum Genet. 139 (1): 103-13
13. Wainschtein P, Jain D, Zheng Z, a kol. 2022. Hodnotenie príspevku vzácnych variantov k dedičnosti komplexných znakov z údajov o sekvencii celého genómu. Nat. Genet. 54 (3): 263-73
14. Verbitsky M, Westland R, Perez A, a kol. 2019. Krajina variácií počtu kópií vrodených anomálií obličiek a močových ciest. Nat. Genet. 51 (1): 117-27
15. Groopman EE, Marasa M., Cameron-Christie S, a kol. 2018. Diagnostická užitočnosť sekvenovania exómu pre ochorenie obličiek. N. Engl. J. Med. 380 (2): 142-51
16. Tan AY, Zhang T, Michael A, a kol. 2018. Somatické mutácie v epiteli obličkových cýst pri autozomálne dominantnej polycystickej chorobe obličiek. J. Am. Soc. Nephrol. 29(8):2139-56
17. Vlasschaert C, McNaughton AJM, Chong M, a kol. 2022. Asociácia klonálnej hematopoézy neurčitého potenciálu s horšou funkciou obličiek a anémiou u dvoch kohort pacientov s pokročilým chronickým ochorením obličiek. J. Am. Soc. Nephrol. 33 (5): 985-95
18. Fu XJ, Nozu K, Kaito H a kol. 2016. Somatický mozaikizmus a variantná frekvencia zistená sekvenovaním novej generácie pri X-viazanom Alportovom syndróme. Eur. J. Hum. Genet. 24(3):387-91
19. Rasouly HM, Groopman EE, Heyman-Kantor R, a kol. 2019. Záťaž kandidátskych patogénnych variantov pre obličkové a genitourinárne poruchy vyplývajúce zo sekvenovania exómu. Ann. Stážista. Med. 170 (1): 11-21
20. Devuyst O, Knoers NVAM, Remuzzi G, a kol. 2014. Zriedkavé dedičné ochorenia obličiek: výzvy, príležitosti a perspektívy. Lancet 383 (9931): 1844–59
21. Ingelfinger JR, Kalantar-Zadeh K, Schaefer F, et al. 2016. Odvrátenie dedičstva ochorenia obličiek – zamerajte sa na detstvo. Kidney Dis. 2(1):46-52
22. Bierzynska A, McCarthy HJ, Soderquest K, a kol. 2017. Genomické a klinické profilovanie národnej kohorty nefrotického syndrómu obhajuje prístup precíznej medicíny k manažmentu chorôb. Kidney Int. 91 (4): 937-47
23. Mikó Á, Menyhárd DK, Kaposi A, et al. 2018. Patogenita NPHS2 p.R229Q závislá od mutácií: príručka pre klinické hodnotenie. Hum. Mutat. 39 (12): 1854-60
24. van der Ven AT, Connaughton DM, Ityel H, a kol. 2018. Celoexómové sekvenovanie identifikuje kauzatívne mutácie v rodinách s vrodenými anomáliami obličiek a močových ciest. J. Am. Soc. Nephrol. 29(9):2348-61
25. Jayasinghe K, Stark Z, Kerr PG, a kol. 2021. Klinický vplyv testovania genómu u pacientov s podozrením na monogénne ochorenie obličiek. Genet. Med. 23:183-91
26. Cornec-Le Gall E, Audrézet MP, Rousseau A, et al. 2016. Skóre PROPKD: nový algoritmus na predpovedanie prežitia obličiek pri autozomálne dominantnej polycystickej chorobe obličiek. J. Am. Soc. Nephrol. 27(3):942-51
27. Hwang YH, Conklin J, Chan W, a kol. 2016. Spresnenie genotypovo-fenotypovej korelácie pri autozomálne dominantnej polycystickej chorobe obličiek. J. Am. Soc. Nephrol. 27 (6): 1861-68
28. Gibson JT, Huang M, Shenelli Croos Cabrera M, et al. 2022. Genotypovo-fenotypové korelácie pre varianty COL4A3–COL4A5 vedúce k substitúciám Gly pri Alportovom syndróme. Sci. Rep. 12:2722
29. Yamamura T, Horinouchi T, Nagano C, et al. 2020. Korelácie genotypu a fenotypu ovplyvňujú odpoveď na lieky zacielené na angiotenzín u japonských pacientov s mužským X-spojeným Alportovým syndrómom. Kidney Int. 98 (6): 1605-14
30. Bekheirnia MR, Reed B, Gregory MC, a kol. 2010. Genotypovo-fenotypová korelácia pri X-viazanom Alportovom syndróme. J. Am. Soc. Nephrol. 21(5):876-83
31. Fahed AC, Wang M, Homburger JR, a kol. 2020. Polygénne pozadie modifikuje penetráciu monogénnych variantov pre genómové podmienky 1. úrovne. Nat. komun. 11(1):3635
32. Wang N, Zheng Y, Zhang L a kol. 2022. Rodina segregujúca letálny deficit primárneho koenzýmu Q10 v dôsledku dvoch nových variantov COQ6. Predné. Genet. 12:811833
33. Bollée G, Harambat J, Bensman A, a kol. 2012. Nedostatok adenín fosforibozyltransferázy. Clin. J. Am. Soc. Nephrol. 7(9):1521-27
34. Kemper MJ, Lemke A. 2018. Liečba genetických foriem nefrotického syndrómu. Predné. Pediatr. 6:72
35. Khan A, Barber DL, Huang J, a kol. 2021. Lentivírusom sprostredkovaná génová terapia Fabryho choroby. Nat. komun. 12(1):1178
36. McCafferty EH, Scott LJ. 2019. Migalastat: prehľad Fabryho choroby. Drugs 79 (5): 543-54
37. Hughes DA, Nicholls K, Shankar SP a kol. 2017. Perorálny farmakologický chaperón migalastat v porovnaní s enzýmovou substitučnou terapiou pri Fabryho chorobe: 18-mesačné výsledky z randomizovanej štúdie fázy III ATTRACT. J. Med. Genet. 54(4):288-96
38. Germain DP, Hughes DA, Nicholls K, a kol. 2016. Liečba Fabryho choroby farmakologickým chaperónom migalastat. N. Engl. J. Med. 375 (6): 545–55
39. Germain DP, Arad M, Burlina A, a kol. 2019. Vplyv enzýmovej substitučnej terapie na klinické výsledky u pacientok s Fabryho chorobou – systematický prehľad literatúry európskym panelom odborníkov. Mol. Genet. Metab. 126 (3): 224-35
40. Adams D, Gonzalez-Duarte A, O'Riordan WD a kol. 2018. Patisiran, RNAi terapeutikum, na dedičnú transtyretínovú amyloidózu. N. Engl. J. Med. 379 (1): 11-21
41. Garrelfs SF, Frishberg Y, Hulton SA, a kol. 2021. Lumasiran, RNAi terapeutikum pre primárnu hyperoxalúriu typu 1. N. Engl. J. Med. 384 (13): 1216–26
42. Gillmore JD, Gane E, Taubel J, a kol. 2021. Úprava génu CRISPR-Cas9 in vivo pre transtyretínovú amyloidózu. N. Engl. J. Med. 385 (6): 493-502
43. Yamamura T., Horinouchi T., Adachi T. a kol. 2020. Vývoj terapie preskokom exónu pre X-spojený Alportov syndróm so skrátenými variantmi v COL4A5. Nat. komun. 11(1):2777
44. Daneshpajouhnejad P, Kopp JB, Winkler CA, et al. 2022. Vyvíjajúci sa príbeh apolipoproteínovej nefropatie L1: koniec začiatku. Nat. Nephrol. 18(5):307-20
Mark D. Elliott,1,2,3 Hila Milo Rasouly,1,2 a Ali G. Gharavi1,2,3
1 Division of Nephrology, Department of Medicine, Columbia University Vagelos College of Physicians and Surgeons, New York, NY, USA; email: ag2239@columbia.edu
2 centrum precíznosť medicína a genomika, oddelenie of medicína, kolumbia univerzita vagelos vysoká škola of lekári a chirurgovia, new york, NY, USA
3 Inštitút pre genomickú medicínu, Columbia University Vagelos College of Physicians and Surgeons, New York, NY, USA






